题目内容
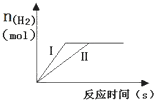 如图表示相同质量的Mg、Al分别跟一定量相同浓度的稀H2SO4溶液反应的情况,
如图表示相同质量的Mg、Al分别跟一定量相同浓度的稀H2SO4溶液反应的情况,下列叙述可能符合图示的有( )
| A、Mg、Al均过量 | B、Mg、Al均不足,硫酸过量 | C、Ⅱ表示Mg与稀H2SO4反应 | D、产生氢气的速率是Ⅰ大于Ⅱ |
分析:镁比铝活泼,与稀硫酸反应时速率较快;反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,以此解答.
解答:解:镁比铝活泼,与稀硫酸反应时速率较快,则曲线Ⅰ表示Mg与稀H2SO4反应,曲线Ⅱ表示Al与稀H2SO4反应;
反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,如金属完全反应,则生成氢气的物质的量不同,由图象可知,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,
故选AD.
反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,如金属完全反应,则生成氢气的物质的量不同,由图象可知,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,
故选AD.
点评:本题主要考查镁、铝的性质,侧重于学生的计算和判断能力的考查,要充分利用图中提供的信息进行分析、判断,从而得出正确的结论,难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
 (2013?崇明县一模)现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.
(2013?崇明县一模)现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.
 (2011?山东)科研、生产中常涉及钠、硫及其化合物.
(2011?山东)科研、生产中常涉及钠、硫及其化合物.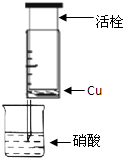 某研究性学习小组设计不同实验方案来研究硝酸的性质.
某研究性学习小组设计不同实验方案来研究硝酸的性质.