题目内容
15.中科院大连化学物理研究所的“煤基甲醇制取低碳烯烃技术(简称DMTO)”荣获2014年度国家技术发明一等奖.DMTO技术主要包括煤的气化、液化、烯烃化三个阶段,相关反应的热化学方程式如下:(i) 煤气化制合成气:C(s)+H2O(g)?CO(g)+H2(g)
(ii) 煤液化制甲醇:CO(g)+2H2(g)?CH3OH(g)
(iii)甲醇制取低碳烯烃:2CH3OH(g)?C2H4(g)+2H2O(g)△H=-11.72kJ•mol-1…(a)
3CH3OH(g)?C3H6(g)+3H2O(g)△H=-30.98kJ•mol-1…(b)
回答下列问题:
(1)已知:C(s)+CO2(g)═2CO(g)△H=+172.5kJ•mol-1,
CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1
反应(i)能自发进行的条件是高温(填“高温”、“低温”或“任何温度”).
(2)反应(ii)中以氢碳[n(H2):n(CO)]投料比为2制取甲醇,温度、压强与CO的平衡转化率关系如图1.
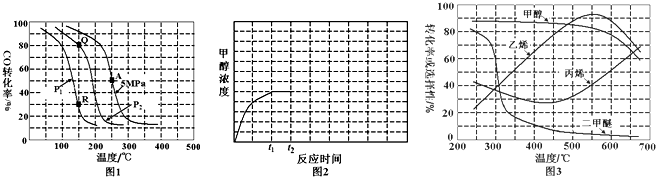
①对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则A点时反应(ii)的Kp=0.16(保留两位有效数字,分压=总压×物质的量分数).
②比较P1小于P2,Kp(Q)等于Kp(R)(填“大于”、“小于”或“等于”).
③工业上常以铜基催化剂,压强5MPa,温度275℃下发生反应(ii),CO转化率可达到40%左右.为提高CO转化率除了可以适当改变反应温度和压强外,还可以采取的措施有提高氢碳比、将甲醇液化分离(写出2个).
④若反应(ii)在恒容密闭容器内进行,T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t2时刻迅速降温到T2,t3时刻体系重新达到平衡.试在图中画出t2时刻后甲醇浓度随时间变化趋势图(在图2中标出t3).
(3)烯烃化阶段:在常压和某催化剂作用下,甲醇的平衡转化率及乙烯、丙烯等物质的选择性(指除了水蒸气以外的产物中乙烯、丙烯等物质的物质的量分数)与反应温度之间的关系如图3.为尽可能多地获得乙烯,控制反应温度为550℃的理由是550℃时甲醇的平衡转化率仍处于较高水平且产物中乙烯的物质的量分数最大.
分析 (1)通过已知:①C(s)+CO2(g)═2CO(g)△H=+172.5kJ•mol-1,
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1,
计算反应(i)C(s)+H2O(g)?CO(g)+H2(g)的△H,反应(i)△S>0,
根据△G=△H-T•△S<0反应自发进行分析;
(2)①A点CO的转化率为0.5,利用三段法求出平衡时各组分的物质的量,然后求出各组分的分压,最后带入Kp表达式计算;
②150℃时,比较Q和R两点对应的CO的转化率的大小,得出平衡移动的方向,从而判断压强的改变;Kp只受温度的影响;
③CO(g)+2H2(g)?CH3OH(g)△H<0,为提高CO转化率除了可以适当改变反应温度和压强外,可考虑浓度对平衡的影响;
④反应(ii)CO(g)+2H2(g)?CH3OH(g)△H<0,t2时降低温度,平衡正向移动,甲醇的浓度增大,直至t3时达到新的平衡时保持不变;
(3)为尽可能多地获得乙烯,要综合考虑甲醇的平衡转化率和乙烯的物质的量分数.
解答 解:(1)已知:①C(s)+CO2(g)═2CO(g)△H=+172.5kJ•mol-1,
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1,
根据盖斯定律可知①+②得C(s)+H2O(g)?CO(g)+H2(g)△H=+172.5kJ•mol-1-41.0kJ•mol-1=+131.5kJ•mol-1>0,反应(i)△S>0,高温时G=△H-T•△S<0反应自发,
故答案为:高温;
(2)①A点CO的转化率为0.5,假设加入1molCO、2molH2,则
CO(g)+2H2(g)?CH3OH(g)
初始:1mol 2mol 0
转化:0.5mol 1mol 0.5mol
平衡:0.5mol 1mol 0.5mol
p(CO)=5MPa×$\frac{0.5mol}{0.5mol+1mol+0.5mol}$=0.75MPa,
p(H2)=5MPa×$\frac{1mol}{0.5mol+1mol+0.5mol}$=2.5MPa,
p(CH3OH)=5MPa×$\frac{0.5mol}{0.5mol+1mol+0.5mol}$=0.75MPa,
Kp=$\frac{p(C{H}_{3}OH)}{p(CO)×{p}^{2}({H}_{2})}$=$\frac{0.75}{0.75×2.{5}^{2}}$=0.16,
故答案为:0.16;
②150℃时,Q点比R点对应的CO的转化率大,平衡正向移动CO的转化率增大,而压强增大,CO(g)+2H2(g)?CH3OH(g)的平衡正向移动,说明P1>P2;Kp只受温度的影响,Q点和R点对应的温度都是150℃,因此Kp(Q)=Kp(R),
故答案为:小于;等于;
③CO(g)+2H2(g)?CH3OH(g)△H<0,为提高CO转化率除了可以适当改变反应温度和压强外,可考虑增大氢气浓度和减小生成物浓度的方法,使平衡正向移动,应该是提高氢碳比和将甲醇液化分离,
故答案为:提高氢碳比;将甲醇液化分离;
④反应(ii)CO(g)+2H2(g)?CH3OH(g)△H<0,t2时降低温度,平衡正向移动,甲醇的浓度增大,直至t3时达到新的平衡时保持不变,对应的图象为 ,
,
故答案为: ;
;
(3)为尽可能多地获得乙烯,要综合考虑甲醇的平衡转化率和乙烯的物质的量分数,550℃时甲醇的平衡转化率仍处于较高水平,而且此温度下产物中乙烯的物质的量分数最大,
故答案为:550℃时甲醇的平衡转化率仍处于较高水平且产物中乙烯的物质的量分数最大.
点评 本题考查了化学反应进行的方向和化学平衡,综合性较强,难度较大,题材背景新,侧重于学生对化学反应原理、变通能力的考查.

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案| A. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硝酸银溶液中加入铁粉:Ag++Fe═Fe2++Ag | |
| C. | 氧化铜与盐酸反应:O2-+2H+═H2O | |
| D. | 碳酸镁与稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
| A. | 水 | B. | 氢氧化钠溶液 | C. | 稀硫酸 | D. | 稀硝酸 |
| A. | 用广泛pH试纸测得氯水的pH=5.2 | |
| B. | 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023 | |
| C. | 在氧化还原反应中,还原剂得到电子总数等于氧化剂失去电子的总数 | |
| D. | Mg在CO2中燃烧生成MgO和C.在该反应条件下,Mg的还原性强于C的 |
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2CO3溶液和NaHCO3溶液都能跟Ca(OH)2溶液反应得到白色沉淀
③钠在常温下不容易被氧化,加热下被氧化成白色固体
④Na2O2可作供氧剂,而Na2O不行
⑤Na2CO3溶液和NaHCO3溶液都呈碱性.
| A. | 都正确 | B. | ②③④⑤ | C. | ②③⑤ | D. | ②④⑤ |
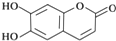
| A. | M的分子式是C9H6O4 | |
| B. | 1molM最多能与2molBr2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |
| A. | Na2O | B. | NaOH | C. | Na2CO3 | D. | Na2CO3•10H2O |
| A. | 在101kPa下氢气的燃烧热△H=-285.5kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| B. | pH=3和pH=5的盐酸各10mL混合,所得溶液的pH=4 | |
| C. | 一定温度下,1L0.50mol/LNH4Cl溶液与2L0.25NH4Cl溶液含NH4+物质的是不同 | |
| D. | 吸热反应“TiO2(g)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |