题目内容
4.下列叙述正确的是( )| A. | 远洋海轮的外壳连接锌块可保护轮船不受腐蚀 | |
| B. | 铁制器件在潮湿空气中生锈 | |
| C. | 镀锌铁片比镀锡铁片更耐腐蚀 | |
| D. | 金属铝在空气中不易被腐蚀 |
分析 A、在原电池中,正极被保护;
B、铁制器具在潮湿的空气中易形成原电池;
C、镀锌铁片中铁做正极;
D、金属铝在空气中形成一层氧化物薄膜.
解答 解:A、在原电池中,正极被保护,负极被腐蚀,故远洋海轮的外壳上连接锌块后,轮船做正极被保护,故A正确;
B、铁制器具在潮湿的空气中易形成原电池,铁做负极被腐蚀,故更易生锈,故B正确;
C、镀锌铁片中铁做正极被保护,而镀锡铁片中铁做负极被腐蚀,故镀锌铁片更耐腐蚀,故C正确;
D、金属铝在空气中形成一层氧化物薄膜,保护内部的铝不被腐蚀,故铝在空气中的耐腐蚀性能较好,故D正确.
故选ABCD.
点评 本题考查了金属的腐蚀和防护,难度不大,应注意的是金属做原电池的正极或电解池的阴极时会被保护.

练习册系列答案
相关题目
14.下列关于化学用语的表述正确的是( )
| A. | 原子核内有8个中子的碳原子${\;}_{8}^{14}$C | |
| B. | 铁红的化学式:FeO | |
| C. | NH4Cl的电子式为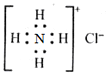 | |
| D. | Ca2+的结构示意图为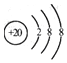 |
12.下列物质其结构具有正四面体构型的是( )
①乙烷、②CHCl3、③甲烷、④四氯化碳、⑤白磷(P4)
①乙烷、②CHCl3、③甲烷、④四氯化碳、⑤白磷(P4)
| A. | ①②③ | B. | ③④⑤ | C. | ①④⑤ | D. | ②③④ |
19.只用一种试剂区别MgSO4、FeSO4、Al2(SO4)3、(NH4)2SO4四种溶液,这种试剂是( )
| A. | BaCl2 | B. | H2SO4 | C. | AgNO3 | D. | NaOH |
9.在恒容密闭容器中通入X并发生反应:2X(g)?Y(g),温度T1、T2下Y的物质的量浓度c(Y)随时间t变化的曲线如图所示,下列叙述正确的是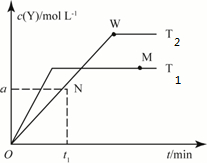 ( )
( )
 ( )
( )| A. | T2下,在0~t1时间内v(X)=$\frac{a}{{t}_{1}}$mol•L-1•min-1 | |
| B. | N点时气体的总压强大于W点时气体的总压强 | |
| C. | M点的正反应速率小于N点的逆反应速率 | |
| D. | W点时再加入一定量Y,平衡后X的转化率减小 |
13.为缓解能源紧张,部分省、市开始试点推广乙醇汽油.下列有关乙醇的叙述中,正确的是( )
| A. | .乙醇和甲醇互为同系物 | B. | .乙醇不能用玉米生产 | ||
| C. | .乙醇的结构简式为C2H6O | D. | .乙醇只能发生取代反应 |
14.NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为2NA | |
| B. | 标准状况下,22.4LSO3所含的分子数为NA个 | |
| C. | 足量铜与11.18mol/L浓硫酸反应可以得到SO2的分子数总数为9NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去电子数为2NA |
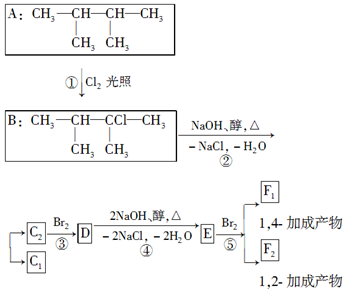
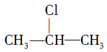 +NaOH$→_{△}^{醇}$CH3-CH═CH2+NaCl+H2O,
+NaOH$→_{△}^{醇}$CH3-CH═CH2+NaCl+H2O,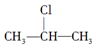 $→_{-NaCl,-H_{2}O}^{NaOH、醇、△}$CH3-CH═CH2下面是几种有机化合物的转化关系:
$→_{-NaCl,-H_{2}O}^{NaOH、醇、△}$CH3-CH═CH2下面是几种有机化合物的转化关系: