题目内容
10.常温下,欲配制密度为1.1g•cm-3、浓度为6mol•L-1的稀盐酸,在体积为100mL、密度为1.19g•cm-3、浓度为12mol•L-1的浓盐酸中需加蒸馏水( )| A. | 101 mL | B. | 100 mL | C. | 200 mL | D. | 120 mL |
分析 根据稀释定律计算稀盐酸的体积,根据m=ρV计算浓盐酸、稀盐酸的质量,可以计算需要计算水的质量,水的密度为1g/mL,进而计算需要加入水的体积.
解答 解:根据稀释定律,稀释前后HCl的物质的量不变,则稀盐酸的体积为:$\frac{100mL×12mol/L}{6mol/L}$=200mL,
则需要加入水的质量为:200mL×1.1g/mL-100mL×1.19g/L=101g,
所以需要加入水的体积为:101g÷1g/mL=101mL,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确稀释过程中溶质的物质的量不变为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. | MgO、Al2O3的熔点很高,可作耐高温材料,工业上用热还原法冶炼对应的金属 | |
| B. | 氢氧化钠、碳酸氢钠、氢氧化铝都可用作抗酸药 | |
| C. | 甲醛的水溶液具有杀菌、防腐的作用,可用于海产品保鲜 | |
| D. | 糖类、油脂、蛋白质、维生素、无机盐和水是人体所需的六大营养素 |
1.雷雨天闪电时空气中有臭氧生成,下列说法不正确的是( )
| A. | O2和O3的相互转化是物理变化 | |
| B. | O2和O3互为同素异形 | |
| C. | 等物质的量的O2和O3含有的质子数不相同 | |
| D. | 在相同的温度与压强下,等体积的O2和O3含有相同的分子数 |
15.下列物质属于天然高分子化合物的是( )
| A. | 淀粉 | B. | 乙酸 | C. | 乙醇 | D. | 甲烷 |
2.下列说法中不正确的是( )
| A. | 在共价化合物中也可能含有离子键 | |
| B. | 非金属之间形成的化学键不一定是共价键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 含有离子键的化合物一定是离子化合物 |
20.下列说法中正确的是( )
| A. | 氮元素是活泼的非金属元素,因此N2的化学性质也很活泼 | |
| B. | 氮气可做焊接金属时的保护气 | |
| C. | NO2溶于水生成硝酸,因此NO2是硝酸的酸酐 | |
| D. | 雷雨时,可增加土壤中硝酸盐类氮肥的含量,此变化不属于氮的固定 |
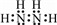 .
. ,N采用sp3杂化方式,粒子空间构型为V形.
,N采用sp3杂化方式,粒子空间构型为V形.
 ;X
;X .
. .
. 外的同分异构体结构体结构简式为
外的同分异构体结构体结构简式为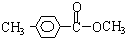 、
、 .
.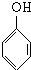 +nHCHO$\stackrel{一定条件}{→}$
+nHCHO$\stackrel{一定条件}{→}$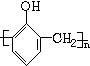 +nH2O.
+nH2O.