题目内容
2.下列说法正确的是( )| A. | MgO、Al2O3的熔点很高,可作耐高温材料,工业上用热还原法冶炼对应的金属 | |
| B. | 氢氧化钠、碳酸氢钠、氢氧化铝都可用作抗酸药 | |
| C. | 甲醛的水溶液具有杀菌、防腐的作用,可用于海产品保鲜 | |
| D. | 糖类、油脂、蛋白质、维生素、无机盐和水是人体所需的六大营养素 |
分析 A.熔点高的物质可作耐火材料,Mg、Al均利用电解法冶炼,MgO的熔点高不能用于Mg的冶炼;
B.NaOH的碱性太强,具有强烈的腐蚀性;
C.甲醛有毒;
D.食物中含有六大类营养物质:蛋白质、糖类、油脂、维生素、水和无机盐.
解答 解:A.MgO、Al2O3的熔点很高,可作耐高温材料,电解熔融氯化镁制备Mg,电解熔融氧化铝制备Al,故A错误;
B.碳酸氢钠、氢氧化铝都可用作抗酸药,而NaOH不能,故B错误;
C.甲醛有毒,不能用于海产品保鲜,故C错误;
D.食物中含有六大类营养物质:蛋白质、糖类、油脂、维生素、水和无机盐,每一类营养物质都是人体所必需的,其中能为人体提供能量的是糖类、油脂和蛋白质,故D正确.
故选D.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质及用途为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
12.下列各组离子,在水溶液中可以大量共存的是( )
| A. | K+、H+、OH-、Cl- | B. | Ba2+、Na+、NO3-、CO32- | ||
| C. | Na+、H+、Cl-、SO42- | D. | Na+、Ag+、Cl-、SO42- |
13.将某NaOH溶液分成两等份,一份敞口放置于空气中,另一份密闭保存,一段时间后,往上述两份溶液中分别加入足量同浓度的稀盐酸,充分反应,消耗盐酸的质量( )
| A. | 密闭保存的那份多 | B. | 敞口放置的那份多 | ||
| C. | 一样多 | D. | 无法比较 |
17.物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是( )
| A. | Na2CO3 NaHCO3 NaCl NH4Cl | |
| B. | Na2CO3 NaHCO3 NH4Cl NaCl | |
| C. | (NH4)2SO4 NH4Cl NaNO3 Na2S | |
| D. | NH4Cl (NH4)2SO4 Na2S NaNO3 |
14.已知常温下,醋酸和NH3•H2O的电离平衡常数均为1.74×10-5 mol•L-1,将醋酸与碳酸氢钠溶液混合后会发生反应:CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O,下列说法正确的是( )
| A. | NH3•H2O加水稀释的过程中,$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{2}•{H}_{2}O)}$减小 | |
| B. | 将10mL浓度均为0.1mol•L-1的CH3COOH和NH3•H2O混合后,c(NH4+)=c(CH3COO-) | |
| C. | NH4HCO3溶液中离子大小关系为:c(HCO3-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 向醋酸中滴加氨水至过量的过程中,水的电离度一直在增大 |
10.常温下,欲配制密度为1.1g•cm-3、浓度为6mol•L-1的稀盐酸,在体积为100mL、密度为1.19g•cm-3、浓度为12mol•L-1的浓盐酸中需加蒸馏水( )
| A. | 101 mL | B. | 100 mL | C. | 200 mL | D. | 120 mL |
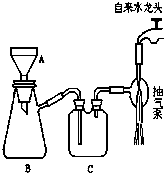 如图所示为减压过滤装置,回答有关问题.
如图所示为减压过滤装置,回答有关问题.