题目内容
8. W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示.已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示.已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )| A. | 简单离子半径:W>X>Z | |
| B. | 最简单气态氢化物的稳定性:Y<Z | |
| C. | 化合物XZW中既含离子键又含共价键 | |
| D. | Y的氧化物能与X的最高价氧化物对应的水化物反应 |
分析 W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,可知W的质子数为8,则W是氧元素;X是短周期元素中原子半径最大的,故X为Na元素;Y的原子半径介于X和W之间,Y的单质是一种常见的半导体材料,所以Y是Si元素;Z的非金属性在同周期元素中最强,原子序数大于Si,故Z为Cl元素,据此解答.
解答 解:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,可知W的质子数为8,则W是氧元素;X是短周期元素中原子半径最大的,故X为Na元素;Y的原子半径介于X和W之间,Y的单质是一种常见的半导体材料,所以Y是Si元素;Z的非金属性在同周期元素中最强,原子序数大于Si,故Z为Cl元素,
A.S2-电子层最多,离子半径最大,O2-、Na+离子电子层结构相同,核电荷数越大,离子半径越小,故离子半径:S2->O2->Na+,故A错误;
B.非金属性Si<Cl,非金属性越强,氢化物越稳定,故B正确;
C.化合物NaClO既含离子键,又含共价键,故C正确;
D.Y的氧化物为二氧化硅,X高价氧化物对应的水化物为NaOH,二氧化硅能与氢氧化钠溶液反应生成硅酸钠与水,故D正确,
故选A.
点评 本题考查结构性质位置关系应用,关键是推断元素,注意对基础知识的理解掌握.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
18.下列溶液中,溶质的物质的量浓度为1mol•L-1的是( )
| A. | 将40gNaOH溶于1L水所得的溶液 | |
| B. | 将22.4LHCl溶于水配成1L溶液 | |
| C. | 1L含2mol K+的K2SO4溶液 | |
| D. | 将0.5mol•L-1的NaNO3溶液100mL加热蒸发掉50g水后的溶液 |
19.由C5H10、C2H4O2、C3H6O2和C6H12O6组成的混合物,经测定含氧元素的质量分数为x,则此混合物中含碳元素的质量分数为( )
| A. | $\frac{6(1-x)}{7}$ | B. | $\frac{1-x}{7}$ | C. | $\frac{3x}{4}$ | D. | 无法计算 |
16.a、b、c、d为短周期元素,a的最外层电子数为内层电子数的2倍,b的最高化合价为最低化合价绝对值的3倍,b与c同周期,c的原子半径小于b,d的M电子层有1个电子,下列叙述错误的是( )
| A. | c元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | 只有d与其他元素生成的化合物都是离子化合物 | |
| D. | a、b、c与氢形成的化合物中化学键均为极性共价键 |
20.能够解释CO2比SiO2的熔、沸点低的原因是( )
| A. | CO2的相对分子质量比SiO2的相对分子质量小 | |
| B. | C-O键能小于Si-O键能 | |
| C. | C的原子半径小于Si | |
| D. | 破坏CO2晶体只需克服分子间作用力,破坏SiO2晶体要破坏Si-O共价键 |
10.向30mL 1mol/L的AlCl3溶液中逐渐加入浓度为4mol/L的NaOH溶液,若产生0.78g白色沉淀,则加入的NaOH溶液的体积可能为( )
| A. | 3mL | B. | 7.5mL | C. | 15mL | D. | 17.5mL |
 如图为人体在某项生理过程中所发生的化学反应示意图.
如图为人体在某项生理过程中所发生的化学反应示意图.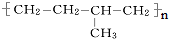 的单体的分子式为CH2=CH2 和CH2=CH-CH3
的单体的分子式为CH2=CH2 和CH2=CH-CH3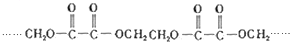 的单体的名称为HOOC-HOOC 和HOCH2-CH2OH.
的单体的名称为HOOC-HOOC 和HOCH2-CH2OH.