题目内容
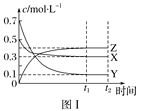
【题目】在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是
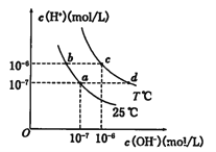
A. 向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CH3COO-)
B. 25℃时,加入CH3COONa可能引起由c向d的变化,升温可能引起a向c的变化
C. T℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
D. b点对应的溶液中大量存在:K+、Ba2+、NO3-、I-
【答案】D
【解析】
A. 向b点对应的醋酸溶液中滴加NaOH溶液至a点,因为a点溶液呈中性,根据电荷守恒规律,所以c(Na+)=c(CH3COO-),故A正确;
B. 25℃时,加入CH3COONa属于强碱弱酸盐,会发生水解使溶液显碱性,使得c(OH-)离子浓度增大,可能引起由c向d的变化,升温溶液中的c(OH-)和c(H+)同时同等程度的增大,所以可能引起a向c的变化,故B正确;C.由图像知 T℃时Kw=10-12,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性,故C正确;D. .由图像知b点对应的溶液呈酸性,溶液中NO3-、I-在酸性条件下发生氧化还原反应,因此 K+、Ba2+、NO3-、I-不能大量存在,故D错误;答案:D。

练习册系列答案
相关题目