题目内容
9.下列各组离子能在溶液中大量共存的是( )| A. | Mg2+、OH-、NO3-、K+ | B. | H+、HCO3-、Ca2+、NO3- | ||
| C. | Cl-、OH-、H+、K+ | D. | Cu2+、SO42-、Na+、Cl- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,以此来解答.
解答 解:A.Mg2+、OH-结合生成沉淀,不能大量共存,故A错误;
B.H+、HCO3-结合生成水和气体,不能大量共存,故B错误;
C.OH-、H+结合生成水,不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
19.(1)下列物质属于弱电解质的是④⑦(填序号,下同);属于非电解质的是②⑤;能导电的物质是①⑧⑩.
①氨水②蔗糖 ③烧碱 ④NH3•H2O ⑤CO2 ⑥氯气 ⑦CH3COOH ⑧铜 ⑨碳酸钙 ⑩石墨
(2)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO${\;}_{3}^{-}$+5SO${\;}_{3}^{2-}$+2H+═I2+5SO${\;}_{4}^{2-}$+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.某同学设计实验如表所示:
①碘酸钾与亚硫酸钠的反应是氧化还原反应(填反应类型).
②该实验的两个目的分别是探究温度对反应速率的影响;探究Na2SO3的浓度对反应速率的影响.
③表中V2=40mL,V1=10mL.
④t1<t2<t3(填“<”、“>”或“=”).
①氨水②蔗糖 ③烧碱 ④NH3•H2O ⑤CO2 ⑥氯气 ⑦CH3COOH ⑧铜 ⑨碳酸钙 ⑩石墨
(2)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO${\;}_{3}^{-}$+5SO${\;}_{3}^{2-}$+2H+═I2+5SO${\;}_{4}^{2-}$+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.某同学设计实验如表所示:
| 0.01mol•L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol•L-1 Na2SO3溶液的体积/mL | H2O的体 积/mL | 实验温 度/℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | t 1 |
| 实验2 | 5 | 5 | 40 | 25 | t 2 |
| 实验3 | 5 | 5 | V2 | 0 | t 3 |
②该实验的两个目的分别是探究温度对反应速率的影响;探究Na2SO3的浓度对反应速率的影响.
③表中V2=40mL,V1=10mL.
④t1<t2<t3(填“<”、“>”或“=”).
4.从海水中提取溴有如下反应5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O.与上述反应在氧化还原原理上最相似的是( )
| A. | 2H2S+SO2═3S↓+2H2O | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2NaBr+Cl2═2NaCl+Br2 | |
| D. | 2FeCl3+H2S═2FeCl2+2HCl+S↓ |
14.下列混合物适用过滤法分离的是( )
| A. | KCl、NaNO3 | B. | 水、酒精 | C. | Na2CO3、CaCO3 | D. | MgSO4、ZnSO4 |
4.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
| A. | H2O2分子中只存在极性键 | B. | NH3的结构式为 | ||
| C. | HCl的电子式为  | D. | H2O中含有离子键 |

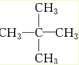 ,名称为2,2-二甲基丙烷(新戊烷).
,名称为2,2-二甲基丙烷(新戊烷).