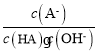��Ŀ����
����Ŀ���輰�仯��������Ȼ��㷺���ڲ�������Ӧ�á�
(1)������Ĥ���������Ĥ��ȽϾ��б��滯ѧ�����ȶ����ŵ㣬�ʵ�����Ĥ�����ڰ뵼�幤ҵ��������NH3��SiH4(����)��һ�������·�Ӧ�Ƶ�3SiH4��4NH3![]() Si3N4��12H2
Si3N4��12H2
�Թ軯þΪԭ���Ʊ�����ķ�Ӧ��ҵ�������£�
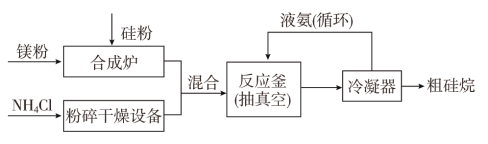
��Ӧԭ����4NH4Cl��Mg2Si![]() 4NH3����SiH4����2MgCl2(��H<0)
4NH3����SiH4����2MgCl2(��H<0)
��NH4Cl�еĻ�ѧ��������________��SiH4�ĵ���ʽΪ______________��
��������������Ĺ�����Һ����������____________________________��
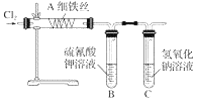
�۰�������Ҫ�Ĺ�ҵԭ�ϣ�д������������������Ӧ����NO�Ļ�ѧ����ʽ��___________________________________________________��ʵ���ҿ�������ͼ��ʾװ����ɸ÷�Ӧ��
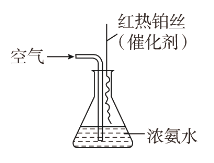
��ʵ������У����۲쵽��ƿ�в�������ɫ�����⣬���ɹ۲쵽�а������ɣ����̵���Ҫ�ɷ���________��
(2)������þ(Mg2Si3O8��nH2O)������ˮ����ҽҩ�Ͽ���������������˿����к�θҺ�ж�����֮�⣬���ɵ�H2SiO3���ɸ������������θ���棬�����䲻���ܴ̼���������þ�����ᷴӦ�Ļ�ѧ����ʽΪ________________________________����0.184 g������þ���뵽50 mL 0.1 mol/L�����У���ַ�Ӧ����ȥ��������0.1 mol/L NaOH��Һ�ζ�ʣ������ᣬ����NaOH��Һ30 mL����Mg2Si3O8��nH2O�е�nֵΪ________��(ע��Mg2Si3O8��Ħ������Ϊ260 g/mol)
���𰸡����Լ�(�ۼ�)�����Ӽ� 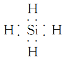 ������������֤��Ӧ�ڳ����½���(�����䡱���¡�����) 4NH3��5O2
������������֤��Ӧ�ڳ����½���(�����䡱���¡�����) 4NH3��5O2![]() 4NO��6H2O NH4NO3(�������) Mg2Si3O8��nH2O��4HCl=3H2SiO3��2MgCl2��(n��1)H2O 6
4NO��6H2O NH4NO3(�������) Mg2Si3O8��nH2O��4HCl=3H2SiO3��2MgCl2��(n��1)H2O 6
��������
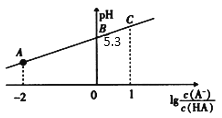
��1�����Ȼ����笠����Ӻ�������֮�������Ӽ���笠������ڲ����ڹ��ۼ������ݵ���ʽ����д�������ش�
�ڸ���Һ�������ʣ���Һ�����ش�
�۰����Ĵ�����������һ��������ˮ��һ��������������Ѹ�ٱ�Ϊ���������������������Ժ�ˮ��Ӧ�õ����ᣬ������ԺͰ�����Ӧ��������泥�
��2��������д��ѧ����ʽ�IJ��裺д��ע�ȣ���ȷ��д����ʽ���ɣ����ݻ�ѧ����ʽ���м��㡣
��1�����Ȼ����笠����Ӻ�������֮�������Ӽ���笠������ڲ����ڹ��ۼ������Լ����ۼ��������Ӽ���������й�ԭ�Ӻ���ԭ��֮���Թ��ۼ���ϣ�����ʽΪ��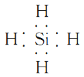 ��
��
��Һ�������ʣ���Һ����������������Ĺ�����Һ���������ǣ�������������֤��Ӧ�ڳ����½��У��ʴ�Ϊ��������������֤��Ӧ�ڳ����½��У������䡱���¡����ɣ���
�۰����Ĵ�����������һ��������ˮ����4NH3��5O2![]() 4NO��6H2O����ʵ������У����۲쵽��ƿ�в�������ɫ�����⣬���ɹ۲쵽�а������ɣ���Ϊһ��������������Ѹ�ٱ�Ϊ���������������������Ժ�ˮ��Ӧ�õ����ᣬ������ԺͰ�����Ӧ����NH4NO3(�������)��
4NO��6H2O����ʵ������У����۲쵽��ƿ�в�������ɫ�����⣬���ɹ۲쵽�а������ɣ���Ϊһ��������������Ѹ�ٱ�Ϊ���������������������Ժ�ˮ��Ӧ�õ����ᣬ������ԺͰ�����Ӧ����NH4NO3(�������)��
��2��������þ�к�θ�ᣨHCl���Ļ�ѧ����ʽΪ��Mg2Si3O8��nH2O��4HCl=3H2SiO3��2MgCl2��(n��1)H2O�����ݻ�ѧ����ʽ����0.184g Mg2Si3O8��nH2O�����ʵ�����x���ã�

![]() =
=![]() �����x=0.0005mol������MgSi3O8nH2O��Ħ��������(260+18n) g/mol =368g/mol��Mg2Si3O8��Ħ������Ϊ260g/mol������18n=108����n=6��
�����x=0.0005mol������MgSi3O8nH2O��Ħ��������(260+18n) g/mol =368g/mol��Mg2Si3O8��Ħ������Ϊ260g/mol������18n=108����n=6��