题目内容
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10mL2% H2O2溶液 | 无 |
② | 10mL5% H2O2溶液 | 无 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_____________________________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。


分析上图能够得出的实验结论是______________________________________。
(1)降低了活化能(2分)
(2)探究浓度对反应速率的影响 (2分)
向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中)(2分)
(3)2H2O2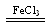 O2↑+2H2O (2分)
O2↑+2H2O (2分)
(4)碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率 (2分)
【解析】
试题分析:(1)催化剂能加快反应速率的原因是能降低反应的活化能。(2)实验①和②,不同的是浓度,所以探究的是浓度对反应速率的影响。由于长时间没有观察到明星现象,说明反应速率很小,可以使用同种同量的催化剂,或同时加热,即将试管放入同一热水浴中。(3)③是过氧化氢在氯化铁做催化剂条件下的反应,故反应写成:2H2O2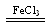 O2↑+2H2O。(4)三个反应中,⑤速率最快,④最慢,说明反应在碱性环境中能增大反应速率,酸性环境能减慢反应速率。
O2↑+2H2O。(4)三个反应中,⑤速率最快,④最慢,说明反应在碱性环境中能增大反应速率,酸性环境能减慢反应速率。
考点:反应速率的影响因素。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案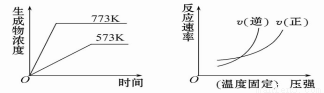
 2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0)
2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0)  2SO2(g) + O2(g) ΔH = + Q2 kJ·mol-1 (Q2>0)
2SO2(g) + O2(g) ΔH = + Q2 kJ·mol-1 (Q2>0) 4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0)
4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0) C(s) + H2O(g) ΔH = + Q4 kJ·mol-1 (Q4>0)
C(s) + H2O(g) ΔH = + Q4 kJ·mol-1 (Q4>0) ②.
②. ③.
③. ④.
④.