题目内容
16.质量相同的下列物质中,含分子数最多的是( )| A. | O3 | B. | CO | C. | Cl2 | D. | NH3 |
分析 质量相同的物质,分子数最多,即物质的量最多,也就是摩尔质量最小,由此分析解答.
解答 解:A、O3的摩尔质量为48g/mol;
B、CO的摩尔质量为28g/mol;
C、Cl2的摩尔质量为71g/mol;
D、NH3的摩尔质量为17g/mol;
所以质量相同的四种物质中,含分子数最多的是氨气,
故选D.
点评 此题是对分子个数的考查,解题的关键是利用相对分子质量与分子质量成正比,分析出质量相同的物质分子个数的多少,属基础性知识考查题.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
6.做化学实验时,必须十分重视实验安全.下列有关实验操作不符合上述要求的是( )
| A. | 在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度 | |
| B. | 加热灼烧后的坩锅放置在实验桌上冷却至室温 | |
| C. | 若不小心打翻酒精灯使酒精着火时,应用湿抹布盖灭 | |
| D. | 蒸馏操作过程中,若发现忘加沸石,应立即停止加热,待烧瓶冷却后再加入沸石 |
7. 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )
 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )| A. | 实验中发生的反应都是化合反应 | B. | 铝是一种较活泼的金属 | ||
| C. | 铝与氧气反应放出大量的热量 | D. | 铝片上生成的白毛是氧化铝 |
4.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 56g金属铁完全反应时失去的电子数为一定为2NA | |
| B. | 18g水所含的电子数目为NA | |
| C. | 在常温常压下,48g氧气和臭氧的混合气体所含的原子数目为3NA | |
| D. | 在常温常压下,11.2L二氧化硫所含的分子数目为0.5 NA |
11.化学与生活、生产、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 铝热反应是炼铁最常用的方法 | |
| B. | 硅是现代光学及光纤制品的基本原料 | |
| C. | 采用“静电除尘”“燃煤固硫”“汽车尾气催化净化”等方法可提高空气质量 | |
| D. | 袋装食品常用生石灰包作为食品的抗氧化剂 |
1.下列说法正确的是( )
| A. | 由一种元素组成的物质一定是单质 | |
| B. | 凡是能电离出H+的化合物都是酸 | |
| C. | 碱能电离出OH-而使溶液显碱性,但溶液显碱性的不一定是碱 | |
| D. | 氨溶于水形成的溶液能导电,所以氨是电解质 |
8.下列诗句或谚语可能与化学反应有关,其中说法正确的是 ( )
| A. | “水乳交融,火上浇油”前者包含物理变化,后者包含化学变化 | |
| B. | “滴水石穿.绳锯木断”不包含化学变化 | |
| C. | “蜡炬成灰泪始干”包含的是物理变化 | |
| D. | 石灰吟中“烈火焚烧若等闲”指的是加热,不包含化学变化 |
10.亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
1测定溶液pH
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).NaNO2溶液中c(HNO2)=c(OH-)-c(H+)(用溶液中其它离子的浓度关系式表示).
2沉淀法
取2mL0.1mol/L两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液.两支试管均产生白色沉淀.分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解.该温度下 Ksp(AgNO2)=2×10-8;
Ksp(AgCl)=1.8×10-10则反应AgNO2(s)+Cl-(aq)?AgCl(s)+NO2-(aq)的化学平衡常数K=$\frac{1000}{9}$(计算结果写成分数)
(二)实验室可用如下装置(略去部分夹持仪器)制备亚硝酸钠.
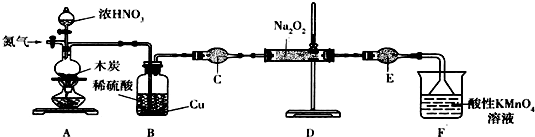
已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排出装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3$\frac{\underline{\;加热\;}}{\;}$CO2+4NO2+2H2O.装置B 的作用是将NO2 气体转变为NO,为后面反应提供原料.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(三)测定亚硝酸钠的含量
称取4.000g制取样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
①第一组实验数据出现异常,造成这种异常的原因可能是ac(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式6H++2MnO4-+5NO2-=2Mn2++5NO3-+3H2O
③根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.(结果保留两位小数)
㈠鉴别NaCl和NaNO2
1测定溶液pH
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).NaNO2溶液中c(HNO2)=c(OH-)-c(H+)(用溶液中其它离子的浓度关系式表示).
2沉淀法
取2mL0.1mol/L两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液.两支试管均产生白色沉淀.分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解.该温度下 Ksp(AgNO2)=2×10-8;
Ksp(AgCl)=1.8×10-10则反应AgNO2(s)+Cl-(aq)?AgCl(s)+NO2-(aq)的化学平衡常数K=$\frac{1000}{9}$(计算结果写成分数)
(二)实验室可用如下装置(略去部分夹持仪器)制备亚硝酸钠.

已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排出装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3$\frac{\underline{\;加热\;}}{\;}$CO2+4NO2+2H2O.装置B 的作用是将NO2 气体转变为NO,为后面反应提供原料.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(三)测定亚硝酸钠的含量
称取4.000g制取样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 次数 | 2 | 3 | ||
| KMnO体积/m | 20.60 | 20.02 | 20.00 | 9.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式6H++2MnO4-+5NO2-=2Mn2++5NO3-+3H2O
③根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.(结果保留两位小数)
11.图Ⅰ是NO2(g)+CO(g)?CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X增大的变化关系曲线如图Ⅱ所示.
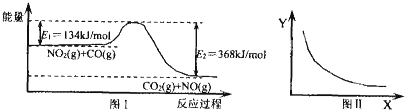
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 该反应的焓变△H=+234 kJ•mol-1 | |
| B. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 | |
| C. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| D. | 若X表示反应时间,则Y表示的可能是混合气体的密度 |