题目内容
3.某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案.回答下列问题:
(1)沉淀A的化学式是SiO2,滤液B的成分是NaAlO2、NaCl、NaOH;
(2)在步骤③中发生的离子反应方程式CO2+2H2O+AlO2-═HCO3-+Al(OH)3↓;
(3)固体C的化学式Al2O3;
步骤④的化学方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$3H2O↑+Al2O3;
(4)写出固体C与NaOH溶液反应的方程式Al2O3+2NaOH=2NaAlO2+H2O;
(5)要想将沉淀和滤液分离,①②③所需要的操作是过滤,写出实验室制备Al(OH)3的离子方程式Al3++3NH3•H2O═Al(OH)3↓+3NH4+.
分析 氧化铝样品中含有氧化铁和二氧化硅,加入过量盐酸氧化铝、氧化铁溶解生成氯化铝、氯化铁溶液,过滤得到沉淀A为二氧化硅,滤液A为氯化铁和氯化铝溶液,加入过量氢氧化钠溶液生成氢氧化铁沉淀和偏铝酸钠溶液,过滤得到沉淀B为Fe(OH)3,滤液为NaAlO2,通入过量二氧化碳气体反应生成氢氧化铝沉淀和碳酸氢钠,过滤得到氢氧化铝沉淀,加热分解生成C为氧化铝,以此解答该题.
解答 解:氧化铝样品中含有氧化铁和二氧化硅,加入过量盐酸氧化铝、氧化铁溶解生成氯化铝、氯化铁溶液,过滤得到沉淀A为二氧化硅,滤液A为氯化铁和氯化铝溶液,加入过量氢氧化钠溶液生成氢氧化铁沉淀和偏铝酸钠溶液,过滤得到沉淀B为Fe(OH)3,滤液为NaAlO2,通入过量二氧化碳气体反应生成氢氧化铝沉淀和碳酸氢钠,过滤得到氢氧化铝沉淀,加热分解生成C为氧化铝,
(1)由以上分析可知沉淀A为SiO2,滤液B的成分为NaAlO2、NaCl、NaOH,故答案为:SiO2;NaAlO2、NaCl、NaOH;
(2)步骤③为偏铝酸钠溶液与二氧化碳反应生成氢氧化铝沉淀,其离子反应为CO2+2H2O+AlO2-═HCO3-+Al(OH)3↓,
故答案为:CO2+2H2O+AlO2-═HCO3-+Al(OH)3↓;
(3)C为Al2O3,步骤④的化学方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$3H2O↑+Al2O3,故答案为:Al2O3;2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$3H2O↑+Al2O3;
(4)氧化铝为两性氧化物,可与氢氧化钠溶液反应,反应的方程式为Al2O3+2NaOH=2NaAlO2+H2O,故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(5)分离液体和不溶性固体,可用过滤的方法,实验室制备Al(OH)3,利用可溶性铝盐和氨水反应,离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,
故答案为:过滤;Al3++3NH3•H2O═Al(OH)3↓+3NH4+.
点评 本题考查镁、铝、硅的化合物的性质,为高考常见题型和高频考点,侧重于学生的分析、实验能力的考查,明确物质的性质及转化中发生的化学反应是解答本题的关键,题目难度不大.

| 组合编号 | A的分子式 | B的分子式 | A和B的体积比V(A):V(B) |
| A. | 0 | B. | $\frac{1}{4}$ | C. | $\frac{1}{2}$ | D. | $\frac{3}{4}$ |
| A. | Hg、Pb、C、Na | B. | Cu、K、S、P | C. | Hg、Pb、Mn、Ni | D. | Br、N、Pb、As |
| A. | 0.18mol | B. | 0.25mol | C. | 0.36mol | D. | 0.55mol |
| A. | 150mL1mol•L-1NaCl溶液 | B. | 100mL2mol•L-1KCl溶液 | ||
| C. | 75mL0.5mol•L-1CaCl2溶液 | D. | 75mL1mol•L-1AlCl3溶液 |
| A. | HF、HCl、HBr、HI的溶沸点依次升高 | |
| B. | 在气态单质分子中,一定存在共价键 | |
| C. | 只含离子键的化合物才是离子化合物 | |
| D. | 在共价化合物中,一定存在着共价键 |
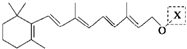
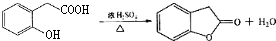
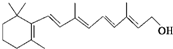 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.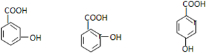 .
.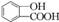 .
. .
. .
.