题目内容
 用下列装置制取并收集纯净的氯气,试回答下列问题:
用下列装置制取并收集纯净的氯气,试回答下列问题:(1)装置A中发生反应的化学方程式为
(2)装置B的作用是
(3)装置C中的试剂为
(4)请指出该装置的不足之处并加以改进
考点:氯气的实验室制法
专题:
分析:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;
(2)浓盐酸易挥发,从A中得到的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水溶解度不大;
(3)浓硫酸具有吸水性,可以干燥氯气,除去氯气中的水蒸气;
(4)氯气有毒,不能直接排放,应用氢氧化钠溶液吸收.
(2)浓盐酸易挥发,从A中得到的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水溶解度不大;
(3)浓硫酸具有吸水性,可以干燥氯气,除去氯气中的水蒸气;
(4)氯气有毒,不能直接排放,应用氢氧化钠溶液吸收.
解答:
解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,化学方程式为:4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O;
故答案为:4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O;
(2)浓盐酸具有挥发性,A制取的氯气中混有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中的溶解度不大,所以可以用B吸收HCl;
故答案为:除去氯气中的氯化氢;
(3)要制取干燥的氯气应用浓硫酸吸收氯气中的水蒸气,故答案为:浓硫酸;
(4)氯气有毒,不能够直接排放,氯气能够与氢氧化钠反应,被氢氧化钠溶液吸收,故答案为:缺少尾气处理装置,应用NaOH溶液吸收多余的氯气.
| ||
故答案为:4HCl(浓)+MnO2
| ||
(2)浓盐酸具有挥发性,A制取的氯气中混有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中的溶解度不大,所以可以用B吸收HCl;
故答案为:除去氯气中的氯化氢;
(3)要制取干燥的氯气应用浓硫酸吸收氯气中的水蒸气,故答案为:浓硫酸;
(4)氯气有毒,不能够直接排放,氯气能够与氢氧化钠反应,被氢氧化钠溶液吸收,故答案为:缺少尾气处理装置,应用NaOH溶液吸收多余的氯气.
点评:本题考查氯气的制备和性质,明确实验的目的与反应的原理是解题的关键,注意二氧化锰只能够氧化浓盐酸,与稀盐酸不反应.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
已知在pH值为4左右的环境中,Cu2+、Fe2+几乎不沉淀,而Fe3+几乎完全沉淀.工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解.欲除去溶液中的杂质离子,下述方法中可行的是( )
| A、加入足量纯Cu粉,过滤 |
| B、向溶液中通入足量H2S,过滤 |
| C、向溶液中通入足量C12,再通NH3调节pH值为4左右,过滤 |
| D、向溶液中通入足量C12,再加纯净CuO粉末调节pH值为4左右,过滤 |
下列化合物中同分异构体数目最少的是( )
| A、丁烷 | B、戊醇 |
| C、戊烯 | D、二溴丙烷 |
当氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的( )
| A、MgCl2 |
| B、NaOH |
| C、MgSO4 |
| D、NaHSO4 |
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质.下列有关说法正确的是( )
| A、糖类物质中只含有C、H、O三种元素 |
| B、蛋白质遇浓硝酸变成紫色 |
| C、油脂在人体中发生水解生成氨基酸 |
| D、糖类、蛋白质都能发生水解反应 |
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( )
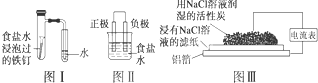

| A、按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B、图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
