题目内容
下列说法错误的是( )
| A.乙醇和乙酸都是常用调味品的主要成分 |
| B.乙醇、乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高 |
| C.乙醇和乙酸都能酸性高锰酸钾溶液褪色 |
| D.乙醇和乙酸之间能发生酯化反应,酯化反应为可逆反应 |
C
解析试题分析:乙醇含有羟基,能使酸性高锰酸钾溶液褪色。乙酸含有羧基,不能使酸性高锰酸钾溶液褪色,选项C不正确,其余选项都是正确的,答案选C。
考点:考查乙醇和乙酸结构、性质的判断
点评:该题是基础性试题的考查,侧重对学生教材基础知识的检验和训练,旨在调动学生的学习兴趣和学习积极性,有利于提高学生应试能力。本题难度不大,熟练记住即可。

练习册系列答案
相关题目
如表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是( )
|
如图为元素周期表中短周期的一部分,下列说法错误的是( )
| X | Y |
| Z | W |
| A、Z的原子序数可能是X的两倍 |
| B、单质的活泼性可能是Y<Z |
| C、X、Z的最高价氧化物对应水化物可能均为强酸 |
| D、分别由Y、W形成的单质可能都是原子晶体 |
化学反应原理中涉及很多常数,下列说法错误的是( )
A、反应N2(g)+3H2(g)
| |||||
| B、化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 | |||||
| C、对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 | |||||
| D、将AgNO3溶液和KCl溶液混合后,若c(Ag+)?c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
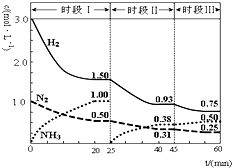 N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )| A、前20分钟反应物的转化率为50% | B、第25分钟改变的条件是将NH3从反应体系中分离出去 | C、时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大 | D、若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |