��Ŀ����
����Ŀ����������(NaN3)��һ�ְ�ɫ�綾���壬��������ȫ���ҵ���Ҫ�ɷ֡�NaN3������ˮ�������Ҵ���ˮ��Һ�������ԣ������ᷢ����Ӧ�������б�ը�Ե��ж�����������⡣ʵ���ҿ������������嶡��(t��BuNO2����t��Bu��ʾ�嶡��)��N2H4������������Һ��Ϸ�Ӧ�Ʊ��������ơ�
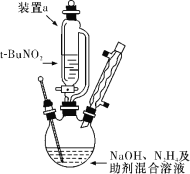
��1������ͼ��ʾ��װ����(����װ����)���з�Ӧ����Ӧ����ʽΪ��t��BuNO2��NaOH��N2H4=NaN3��2H2O��t��BuOH
��װ��a�IJ�ܵ�������________________��
�ڸ÷�Ӧ������¶���65 �������õ�ʵ���ʩ��_______________��
�۷�Ӧ����Һ��0 ������ȴ���д���������������ˣ����þ���ʹ����ˮ�Ҵ�ϴ�ӡ��Խ��͵����¹��˺�ʹ����ˮ�Ҵ�ϴ�Ӿ����ԭ����_________��
��2�����ʼ���
�ٳ�ȡ2.0 g�����������������100 mL��Һ������ȡ10.00 mL��Һ����ƿ�С�
���õζ��ܼ���0.10 mol��L��1���������[(NH4)2Ce(NO3)6]��Һ40.00 mL�����ķ�ӦΪ[2(NH4)2Ce(NO3)6��2NaN3=4NH4NO3��2Ce(NO3)3��2NaNO3��3N2��](�������ʾ������뷴Ӧ)��
��3����ַ�Ӧ����Һϡ�Ͳ��ữ������2���ڷ�����ָʾҺ������0.10 mol��L��1���������[(NH4)2Fe(SO4)2]Ϊ��Һ���ζ�������Ce4�����յ�ʱ���ı���Һ20.00 mL(�ζ�ԭ����Ce4����Fe2��=Ce3����Fe3��)�������֪�������Ƶ���������Ϊ_______(����2λ��Ч����)��
��4�����������ж�������ʹ�ô���������Һ�Ժ��е������Ƶ���Һ�������٣���Ӧ����Һ����������ǿ���Ҳ�����ɫ��ζ�������壬��д����Ӧ�����ӷ���ʽ��____________________��
���𰸡�ƽ��ѹǿ��ʹҺ��˳������ ˮԡ���� ����NaN3���ܽ�ȣ����ٲ�����ʧ 65% ClO����2N3-��H2O=Cl����2OH����3N2��
��������
��1����װ��a�IJ�ܵ������ǣ�ƽ��ѹǿ��ʹҺ��˳�����£�
�ڼ����¶ȵ���100�棬������ˮԡ���ȣ�
����֪��NaN3������ˮ�������Ҵ�����
��3���ܼ�Ce4��Ϊ0.10 mol��L-1��0.04 L=0.004 mol���ֱ���Fe2����N3����Ӧ��������Fe2����1��1��Ӧ����0.10 mol��L-1��0.02 L=0.002 mol������N3����1��1��ӦҲΪ0.002 mol����10 mL��ȡ��Һ����0.002 mol N3����
��4������������Һ�����������Һ��Ӧ����������ǿ�������������ƣ��Ҳ�����ɫ��ζ�������壬Ϊ������ͬʱ�����Ȼ��ơ�
��1����װ��a�IJ�ܵ������ǣ�ƽ��ѹǿ��ʹҺ��˳�����£�
�ڼ����¶ȵ���100�棬������ˮԡ���ȣ�
�۵����¹��˺�ʹ����ˮ�Ҵ�ϴ�Ӿ����ԭ���ǣ���������������ˮ�������Ҵ����������ܽ�Ƚ��ͣ�����NaN3���ܽ�ȣ����ٲ�����ʧ��
��3���ܼ�Ce4��Ϊ0.10 mol��L-1��0.04 L=0.004 mol���ֱ���Fe2����N3����Ӧ��������Fe2����1��1��Ӧ����0.10 mol��L-1��0.02 L=0.002 mol������N3����1��1��ӦҲΪ0.002 mol����10 mL��ȡ��Һ����0.002 mol N3����ԭ2.0 g�����������������100 mL��Һ����0.02 mol��1.3 g NaN3��������Ʒ��������Ϊ65%��
��4������������Һ�����������Һ��Ӧ����������ǿ�������������ƣ��Ҳ�����ɫ��ζ�������壬Ϊ������ͬʱ�����Ȼ��ƣ����ݵ�ʧ�����غ㡢����غ��ԭ���غ㣬���ӷ�Ӧ����ʽΪ��ClO��+2N3��+H2O=Cl��+2OH��+3N2������

����Ŀ����ѧ��Ӧ���ʺ���������������������ء�
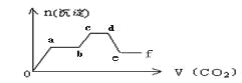
(1)ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����400mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼������ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL������״���� | 100 | 240 | 464 | 576 | 620 |
����һʱ��η�Ӧ�������___min����0��1��1��2��2��3��3��4��4��5������Ӧ��ʼ��Ӧ�����������ԭ����__��
����3��4����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����__________������Һ������䣩��
(2)��һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʣ�����Ϊ�����е���_��
A������ˮ B��KCl��Һ C��KNO3��Һ D��CuSO4��Һ
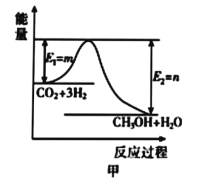
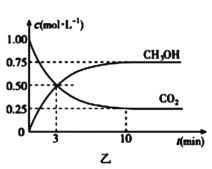
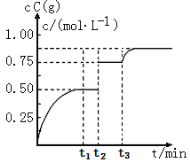
(3)ij�¶�����4L�ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯������ͼ
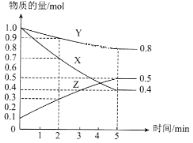
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��__________��
�ڸ÷�Ӧ�ﵽƽ��״̬�ı�־��__________��
A��X��Y��Z�ķ�Ӧ������� B�������������ܶȱ��ֲ��� C������������ѹǿ���ֲ��� D������3molX��ͬʱ����1mol Y
��2min��X��ת����Ϊ__________��