题目内容
写出下列物质或微粒的电子式
(1)Ar (2)CO2 (3)NaCl (4 )KOH (5)N2 (6)NH4+ .
(1)Ar
考点:电子式
专题:
分析:简单阳离子的电子式为其离子符合,复杂的阳离子电子式除应标出共用电子对、非共用电子对等外,还应加中括号,并在括号的右上方标出离子所带的电荷.
无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷.
离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起.对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写;
以共价键形成的物质,必须正确地表示出共用电子对数,并满足每个原子的稳定结构,共价化合物电子式的书写,一般为正价者在前.对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边;
无论是简单阴离子,还是复杂的阴离子,都应标出电子对等,还应加中括号,并在括号的右上方标出离子所带的电荷.
离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后.)拼在一起.对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写;
以共价键形成的物质,必须正确地表示出共用电子对数,并满足每个原子的稳定结构,共价化合物电子式的书写,一般为正价者在前.对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边;
解答:
解:(1)Ar为稀有气体的原子,最外层为8个电子,其电子式为: ,
,
故答案为: ;
;
(2)CO2是共价化合物,碳原子有四个电子分别和氧原子形成两对共用电子对,电子式为 ,故答案为:
,故答案为: ;
;
(3)氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为 ;故答案为:
;故答案为: ;
;
(4)KOH:氢氧化钾为离子化合物,氢氧根离子需要标出最外层电子,氢氧化钾的电子式为: ,
,
故答案为: ;
;
(5)N2:氮气分子中存在1个氮氮三键,氮气的电子式为: ,
,
故答案为: ;
;
(6)NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为: ,
,
故答案为: ;
;
 ,
,故答案为:
 ;
;(2)CO2是共价化合物,碳原子有四个电子分别和氧原子形成两对共用电子对,电子式为
 ,故答案为:
,故答案为: ;
;(3)氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为
 ;故答案为:
;故答案为: ;
;(4)KOH:氢氧化钾为离子化合物,氢氧根离子需要标出最外层电子,氢氧化钾的电子式为:
 ,
,故答案为:
 ;
;(5)N2:氮气分子中存在1个氮氮三键,氮气的电子式为:
 ,
,故答案为:
 ;
;(6)NH4+是多原子构成的阳离子,电子式要加中括号和电荷,其电子式为:
 ,
,故答案为:
 ;
;
点评:本题考查了电子式的书写,题目难度中等,试题涉及的题量较大,注意掌握电子式的概念及正确的书写方法,明确原子、阴阳离子的电子式的区别.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列各组试剂,不用外加任何试剂,只用胶头滴管和试管就能鉴别的是( )
| A、NaHCO3溶液和澄清石灰水 |
| B、Na2CO3溶液和CaCl2溶液 |
| C、Na2CO3溶液和盐酸 |
| D、NaHCO3溶液和盐酸 |
有X、Y、Z三种元素,已知X 原子的特征电子构型是nsn,Y元素原子的M层上有两个未成对电子,Z元素原子L层的p轨道上有一对已成对电子,由这三种元素组成的化合物的化学式不可能是 ( )
| A、X3YZ4 |
| B、X4YZ4 |
| C、X2YZ3 |
| D、XYZ4 |
正电子和负质子等都属于反粒子,它们跟普通电子、质子的质量、电荷量均相等,而电性相反.科学家设想在宇宙的某些部分可能存在完全由反粒子构成的物质--反物质.1997年年初和年底,欧洲和美国的科研机构先后宣布:他们分别造出9个和7个反氢原子,这是人类探索反物质的一大进步.你推测反氢原子的结构是( )
| A、由1个带正电荷的质子和由1个带负电荷的电子构成 |
| B、由1个带负电荷的质子和由1个带正电荷的电子构成 |
| C、由1个带负电荷的质子和由1个带负电荷的电子构成 |
| D、由1个不带电的中子和由1个带负电荷的电子构成 |
下列粒子的质子数大于电子数,电子数等于中子数的是( )
| A、H+ |
| B、OH- |
| C、Na+ |
| D、NH4+ |
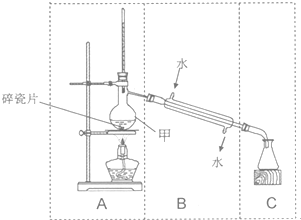
 乙醇、1,2-二溴乙烷、乙醚的有关物理性质如表所示.
乙醇、1,2-二溴乙烷、乙醚的有关物理性质如表所示.