��Ŀ����
A��B��C��X����ѧ��ѧ�������ʣ����ɶ�����Ԫ����ɣ�ת����ϵ��ͼ��ʾ����A��B��C����ɫ��Ӧ���ʻ�ɫ��ˮ��Һ��Ϊ���ԡ�
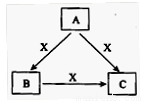
��A�������еĻ�ѧ����_____________, X���ڵľ���������_________��
�ڽ�4.48 L����״���£�Xͨ��100mL 3 mol��L A��ˮ��Һ����Һ�з��������ӷ�Ӧ����ʽΪ______��
����Ȼ���д���B��C��H2O��һ�������ᾧ���ɵĹ��塣ȡһ�����ù�������ˮ���100mL��Һ����������н��������ӵ�Ũ��Ϊ0.5 mol��L����ȡ��ͬ�����Ĺ�����������أ�ʣ����������Ϊ______ g
��1�����Ӽ����ۼ� ���Ӿ���
(2)2CO2 + 3OH- = CO32- + HCO3- + H2O
(3)2.65
��������
�����������1��A��B��C����ɫ��Ӧ���ʻ�ɫ��ˮ��Һ��Ϊ���ԣ�˵��A��B��C�о�����NaԪ�أ���ҺΪ���Եĺ���Ԫ�صĻ�����һ�����������ơ�̼���ơ�̼�����ƣ����������������̼��Ӧ����̼���ƻ�̼�����ƣ�̼�����Ʒֽ�����̼���ƣ�����A���������ƣ�B��̼�����ƣ�C��̼���ƣ�X�Ƕ�����̼���������������к������Ӽ������ۼ���������̼�ľ����������ڷ��Ӿ��壻
��2��4.48L��״���µĶ�����̼�����ʵ�����0.2mol����0.3mol�������Ʒ�Ӧ��0.2mol��Ԫ������0.2mol�������Ʒ�Ӧ����0.2mol��̼�����ƣ�ʣ��0.1mol������������0.1mol̼�����Ʒ�Ӧ����0.1mol̼����������Һ�м���̼��������Ҳ��̼���������ɣ��Ҷ��ߵ����ʵ���֮����1:1���ɴ�д�����ӷ���ʽΪ2CO2 + 3OH- = CO32- + HCO3- + H2O��
��3��̼������̼�������е��������������ӣ�����������ʱ��ʣ�������̼���ƣ�������Ԫ���غ��̼���Ƶ����ʵ�����0.5mol/L��0.1L/2=0.025mol������ʣ������������0.025mol��106g/mol=2.65g��
���㣺�������ʵ��ƶϣ������ļ��㣬��Ԫ�ػ�����Ļ�ѧ����

 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д���14�֣�����������ͨ���÷��������������Ʊ����������ı����Ƚ��ȶ������������������ϵ�֧�����۳��̣���ǿ������ʱ�����ն��������Ȼ���ijͬѧ�üױ���������Ӧ�Ʊ������ᡣ
��Ӧԭ����

��Ӧ�Լ������������������
���� | ��Է� ������ | ��״ | �۵� | �е� | �ܶ� | �ܽ�� | ||
ˮ | �Ҵ� | ���� | ||||||
�ױ� | 92 | ��ɫҺ����ȼ�ӷ� | -95 | 110.6 | 0.8669 | ���� | ���� | ���� |
������ | 122 | ��ɫƬ״����״���� | 122.4 | 248 | 1.2659 | �� | ���� | ���� |
��Ҫʵ��װ�ú��������£�

ʵ�鷽����һ�����ļױ���KMnO4��Һ����ͼ1װ���У���90��ʱ�� ��Ӧһ��ʱ�䣬��ֹͣ��Ӧ�����������̷����������ͻ���δ��Ӧ�ļױ���

��1����ɫҺ��A�Ľṹ��ʽΪ ��������Ϊ ��
��2�������Һ����ɫ��Ҫ�ȼ���������أ�Ȼ���ټ���Ũ�����ữ������������ص�Ŀ���� ��
��3�����й�����������װ����ʹ����ȷ���� ��
A�����˿��Լӿ�����ٶȣ��õ��ϸ���ij���
B����װ�綯������ʱ���������¶˲�����������ƿ�ס��¶ȼƵȽӴ�
C��ͼ1��������װ��Ӧ����ֱ�Ӽ��ȵķ���
D����������ˮ���������½��ϳ�
��4����ȥ�����ڱ������еļױ�Ӧ�ȼ��� ����Һ��ˮ���ټ��� ��Ȼ����ˣ����T�ɵõ������ᡣ
��5�����Ȳⶨ����ȡ1.220g��Ʒ�����100ml��Һ��ȡ����25.00ml��Һ�����еζ� ������KOH���ʵ���Ϊ2.4��10-3mol����Ʒ�б�������������Ϊ ��
��ͬ�¶���,�����Ϊ0.25 L�����������ܱ������з������淴Ӧ��
X2(g) + 3Y2(g) 2XY3(g) ��H=-92.6 kJ.mol-1
2XY3(g) ��H=-92.6 kJ.mol-1
ʵ���÷�Ӧ����ʼ���ﵽƽ��ʱ���й��������±���ʾ��
���� ��� | ��ʼʱ���������ʵ���/mol | �ﵽƽ���ʱ�� | ��ƽ��ʱ��ϵ�����ı仯 | ||
X2 | Y2 | XY3 | |||
�� | 1 | 3 | 0 | 2���� | ����46.3kJ |
�� | 0.4 | 1.2 | 1.2 | / | Q(Q>0) |
������������ȷ����
A���������з�Ӧ�ӿ�ʼ���մ�ƽ��ʱ��XY3��ʾ�ķ�Ӧ����Ϊv(XY3)=1/30 moI.L-l��s-1
B��ƽ��ʱ������������XY3�����ʵ���Ũ�����
C���������з�Ӧ�ﵽƽ��ʱ���յ�����ΪQ
D�����������Ϊ0.3L�����ƽ��ʱ�ų�����������46.3kJ
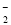 ��2H2O
��2H2O