题目内容
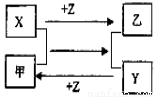
(12分). A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上非金属元素中所形成的最简单气态氢化物稳定性最弱的是(填化学式) ;E、F、L、I所形成的简单离子的半径由大到小的顺序为(用离子符号表示) 。
(2)由L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为 。固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式 。
(3)在10 L的密闭容器中,通入2 mol LD2气体和1 mol D2气体,一定温度下反应后生成LD3气体,当反应达到平衡时,D2的浓度为0.01 mol·L-1,同时放出约177 KJ的热量,则平衡时LD2的转化率为 ;该反应的热化学方程式为: 。
(12分). (每空2分)
(1) SiH4 , S2->Cl->Na+>Al3+ ;
(2) 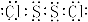 , Na2O2 + Na2S + 2H2O = S + 4Na++4OH- ;
, Na2O2 + Na2S + 2H2O = S + 4Na++4OH- ;
(3) 90% , 2SO2(g)+ O2(g)= 2SO3(g) △H = - 196.7 KJ/mol 。
【解析】
试题分析:(1)B、C、D为同一周期,且原子序数处于9种元素的中间,所以三种元素是第二周期元素,A是第一周期元素,所以A是H元素;E、F、G、L、I是第三周期元素,A与E同主族,则E是Na元素;C和D的最外层电子数之和是11,第二周期元素中最外层电子数之和是11的元素可能是C与F或N与O,若为C与F元素,F的质子数比D多5,则F是Si,C、D、F三种元素的原子序数之和为29,与题意不符,所以C是N元素,D是O元素,则F是Al元素,B与G、D与L分别为同一主族,则B是C元素,G是Si元素,L是S元素,所以I是Cl元素。
(1)以上非金属元素中所形成的最简单气态氢化物稳定性最弱的也即非金属性最弱的是Si,对应的氢化物的化学式为SiH4;E、F、L、I所形成的简单离子中,E、F的离子的核外有2个电子层,而L、I的离子核外有3个电子层,半径随电子层数增多而增大,随核电荷数增多而减小,所以四种离子的半径由大到小的顺序为S2->Cl->Na+>Al3+;
(2)S与Cl形成的原子个数比1:1的化合物X,化合物X中各原子均满足8电子的稳定结构,所以X的化学式为S2Cl2,电子式为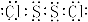 ;固体化合物E2D2投入到化合物E2L的水溶液中,即过氧化钠与硫化钠的反应,过氧化钠与水反应生成氢氧化钠与氧气,氧气与硫化钠溶液发生氧化还原反应生成的沉淀是S单质和氢氧化钠,所以离子方程式为Na2O2 + Na2S + 2H2O = S + 4Na++4OH-;
;固体化合物E2D2投入到化合物E2L的水溶液中,即过氧化钠与硫化钠的反应,过氧化钠与水反应生成氢氧化钠与氧气,氧气与硫化钠溶液发生氧化还原反应生成的沉淀是S单质和氢氧化钠,所以离子方程式为Na2O2 + Na2S + 2H2O = S + 4Na++4OH-;
(3)二氧化硫与氧气反应生成三氧化硫,由题意可知,二氧化硫的起始浓度是0.2mol/L,氧气的起始浓度是0.1mol/L,平衡时氧气的浓度是0.01 mol·L-1,则平衡时二氧化硫的浓度是0.02 mol·L-1,所以二氧化硫的转化率是(0.2-0.02) mol·L-1/0.2mol/L=90%;2mol的二氧化硫转化1.8mol时放出177kJ的热量,则2mol二氧化硫完全转化时放出的热量是177kJ/0.9=196.7kJ,所以该反应的热化学方程式为2SO2(g)+ O2(g)= 2SO3(g) △H = - 196.7 KJ/mol
考点:考查元素的推断,元素及其化合物的性质,电子式的书写,方程式的书写,转化率的计算等

 阅读快车系列答案
阅读快车系列答案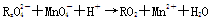 变化过程中,0.2 mol
变化过程中,0.2 mol 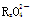 参加反应,共转移0.4 mol 电子。
参加反应,共转移0.4 mol 电子。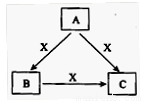
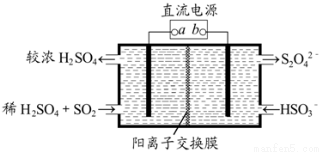
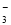 +2H++e-===S2O
+2H++e-===S2O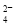 +2H2O
+2H2O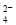 +4H+
+4H+