题目内容
完成下列化学方程式或离子方程式.
①过氧化钠与二氧化碳反应化学方程:
②铝和NaOH溶液反应化学方程式:
③氢氧化铝和NaOH溶液反应离子方程式:
④硫酸亚铁与氢氧化钠溶液离子方程式:
⑤FeCl3和Cu反应离子方程式: .
①过氧化钠与二氧化碳反应化学方程:
②铝和NaOH溶液反应化学方程式:
③氢氧化铝和NaOH溶液反应离子方程式:
④硫酸亚铁与氢氧化钠溶液离子方程式:
⑤FeCl3和Cu反应离子方程式:
考点:离子方程式的书写,化学方程式的书写
专题:离子反应专题
分析:①过氧化钠与二氧化碳反应生成碳酸钠和氧气;
②铝和NaOH溶液反应生成偏铝酸钠和氢气;
③氢氧化铝和NaOH溶液反应生成偏铝酸钠和水,氢氧化铝需要保留化学式;
④硫酸亚铁与氢氧化钠溶液反应生成氢氧化亚铁和硫酸钠,氢氧化亚铁需要保留化学式;
⑤FeCl3和Cu反应生成氯化亚铁、氯化铜.
②铝和NaOH溶液反应生成偏铝酸钠和氢气;
③氢氧化铝和NaOH溶液反应生成偏铝酸钠和水,氢氧化铝需要保留化学式;
④硫酸亚铁与氢氧化钠溶液反应生成氢氧化亚铁和硫酸钠,氢氧化亚铁需要保留化学式;
⑤FeCl3和Cu反应生成氯化亚铁、氯化铜.
解答:
①过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2↑,
故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;
②铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
③氢氧化铝为两性氢氧化物,能够与强碱溶液反应,氢氧化铝与氢氧化钠反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
④硫酸亚铁与氢氧化钠溶液反应的离子方程式为:Fe2++2OH-=Fe(OH)2↓,
故答案为:Fe2++2OH-=Fe(OH)2↓;
⑤FeCl3和Cu反应离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+.
故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;
②铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
③氢氧化铝为两性氢氧化物,能够与强碱溶液反应,氢氧化铝与氢氧化钠反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
④硫酸亚铁与氢氧化钠溶液反应的离子方程式为:Fe2++2OH-=Fe(OH)2↓,
故答案为:Fe2++2OH-=Fe(OH)2↓;
⑤FeCl3和Cu反应离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+.
点评:本题考查了离子方程式、化学方程式的书写,题目难度中等,明确离子方程式、化学方程式的书写原则为解答关键,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
下列关于物质的性质与应用相对应的是( )
| A、氯气有毒,不可用作自来水的杀菌消毒 |
| B、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C、硫粉具有还原性,可用于制造黑火药 |
| D、Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
下列离子方程式书写正确的是( )
| A、将Na加入到CuSO4溶液中:2Na+Cu2+=Cu+2Na+ |
| B、向Ba(OH)2溶液中通入过量CO2:CO2+OH-=HCO3- |
| C、向NaHSO4溶液加入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、向氯化铝溶液中加入足量氨水:Al3++4NH3?H2O=AlO2-+2H2O+4NH4+ |
下列解释实验事实的化学方程式或离子方程式不正确的是( )
| A、氯气用于自来水的杀菌消毒:Cl2+H2O═HCl+HClO |
| B、将“NO2球”浸泡在热水中,颜色变深:2NO2(g)═N2O4(g)△H<0 |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液,至溶液呈中性:OH-+Ba2++H++SO42-=BaSO4↓+H2O |
| D、铜片溶解在KNO3和稀硫酸的混合液中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
下列有机物中,属于高分子化合物的是( )
| A、油脂 | B、淀粉 | C、葡萄糖 | D、果糖 |
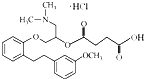 ),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下:
),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下: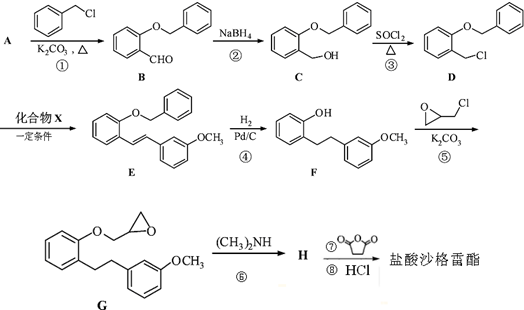
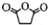 是丁二酸酐
是丁二酸酐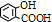 ),分析该制备过程的关键所在
),分析该制备过程的关键所在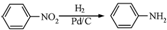 .化合物
.化合物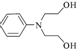 是合成抗癌药物的中间体,请写出以
是合成抗癌药物的中间体,请写出以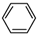 和
和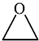 为原料制备该化合物的合成路线流程图(无机试剂任用).
为原料制备该化合物的合成路线流程图(无机试剂任用).

