题目内容
关于原电池的叙述正确的是( )
| A、构成原电池的正极和负极必须是两种不同金属 |
| B、在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0,设计成原电池 |
| C、在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D、原电池工作时,正极和负极上发生的都是氧化还原反应 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.构成原电池的两极可以是两种活泼性不同的金属或金属与非金属;
B.能自发进行的氧化还原反应可设计成原电池;
C.铅、银与盐酸都不反应,不能形成原电池;
D.原电池工作时,正极发生还原反应,负极发生氧化反应.
B.能自发进行的氧化还原反应可设计成原电池;
C.铅、银与盐酸都不反应,不能形成原电池;
D.原电池工作时,正极发生还原反应,负极发生氧化反应.
解答:
解:A.构成原电池的两极可以是两种活泼性不同的金属或金属与非金属导体,如石墨等,故A错误;
B.CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0为氧化还原反应,且属于放热反应,可设计成原电池反应,故B正确;
C.铅、银与盐酸都不反应,不能形成原电池,故C错误;
D.原电池工作时,正极发生还原反应,负极发生氧化反应,故D错误.
故选B.
B.CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0为氧化还原反应,且属于放热反应,可设计成原电池反应,故B正确;
C.铅、银与盐酸都不反应,不能形成原电池,故C错误;
D.原电池工作时,正极发生还原反应,负极发生氧化反应,故D错误.
故选B.
点评:本题考查原电池知识,为高频考点,注意把握原电池的组成条件以及工作原理,易错点为C,难度不大.

练习册系列答案
相关题目
设NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温下,1L0.1mol/L的NH4NO3溶液中含氮原子数为0.2NA |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| C、22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L |
下列物质中属于有机物的是( )
| A、碳酸 | B、二氧化碳 |
| C、乙醇汽油 | D、甲烷 |
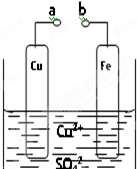 某学习小组为研究原电池原理,设计如图装置.叙述错误的是( )
某学习小组为研究原电池原理,设计如图装置.叙述错误的是( )| A、a和b不连接时,铁片上会有金属铜析出,质量增重 |
| B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu |
| C、a和b用导线连接时,Cu2+移向Fe,电子在溶液中从负极移向正极 |
| D、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
下列说法正确的是( )
| A、液态HCl、固态NaCl均不导电,所以HCl、NaCl是非电解质 | ||
| B、强电解质溶液的导电性一定比弱电解质溶液的导电性强 | ||
| C、蔗糖、酒精在液态或水溶液里均不导电,所以它们是非电解质 | ||
D、NaHSO4无论在水溶液里还是在熔融状态下都可以电离出Na+、H+和SO
|
常温下,0.1mol?L-1某一元酸(HA)溶液中c(OH-)=1×10-11mol?L-1,下列叙述正确的是( )
| A、该一元酸溶液的pH=1 | ||
| B、该溶液中水的离子积常数为1×10-22 | ||
| C、该溶液中HA的电离度为 0.1% | ||
D、若加水稀释,则
|
下列溶液中溶质的物质的量浓度为1mol/L的是( )
| A、将40gNaOH溶解在1L水中 |
| B、将1L10mol/L的浓盐酸加入9L水中 |
| C、将常温常压下22.4L HCl气体溶于水配成1L溶液 |
| D、将40g NaOH溶解在少量水中,再加蒸馏水定容到溶液体积为1L |