题目内容
V L浓度为1.000 mol?L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
| A、通入标准状况下的HCl气体22.4V L |
| B、将溶液加热浓缩到0.5V L |
| C、加入10.00 mol?L-1的盐酸0.2V L,再稀释至1.5V L |
| D、加入V L 3 mol?L-1的盐酸混合均匀 |
考点:物质的量浓度的相关计算
专题:
分析:A、根据C=
计算判断;
B、根据加热时,盐酸会挥发;
C、根据C=
计算判断;
D、根据浓稀盐酸混合后体积是否变化判断.
| n |
| V |
B、根据加热时,盐酸会挥发;
C、根据C=
| c1V1+c2V2 |
| V |
D、根据浓稀盐酸混合后体积是否变化判断.
解答:
解:A、标准状况下的HCl气体22.4VL,物质的量是Vmol,VL浓度为1mol?L-1的盐酸中HCl的物质的量为Vmol,但无法计算通入氯化氢后溶液的体积,故A错误;
B、加热浓缩盐酸时,导致盐酸挥发,溶质的物质的量偏小,故B错误;
C、VL浓度为0.5mol?L-1的盐酸的物质的量是0.5Vmol,10mol?L-1的盐酸0.1VL的物质的量是Vmol,再稀释至1.5VL,所以c=
=2mol/L,故C正确;
D、浓稀盐酸混合后,溶液的体积不是直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,故D错误.
故选C.
B、加热浓缩盐酸时,导致盐酸挥发,溶质的物质的量偏小,故B错误;
C、VL浓度为0.5mol?L-1的盐酸的物质的量是0.5Vmol,10mol?L-1的盐酸0.1VL的物质的量是Vmol,再稀释至1.5VL,所以c=
| Vmol+2Vmol |
| 1.5VL |
D、浓稀盐酸混合后,溶液的体积不是直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,故D错误.
故选C.
点评:本题考查了物质的量浓度的计算,难度不大,易错选项是D,注意密度不同的溶液混合后,溶液的体积不能直接加和.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案
相关题目
某烷烃的结构简式为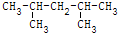 ,它的正确命名是( )
,它的正确命名是( )
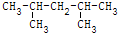 ,它的正确命名是( )
,它的正确命名是( )| A、2-甲基-4-乙基戊烷 |
| B、4-甲基-2-乙基戊烷 |
| C、2,4-二甲基己烷 |
| D、3,5-二甲基己烷 |
下列有关金属腐蚀与防护的说法不正确的是( )
| A、当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D、可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀 |
下列说法中错误的是( )
| A、同一原子中一定没有能量相同的电子 |
| B、6C的电子排布式1s22s22px2违反了洪特规则 |
| C、电子排布式1s22s22p63s23p63d3违反了能量最低原理 |
| D、电子排布式1s22s22p63s23p10违反了泡利原理 |
小明体检的血液化验单中,葡萄糖为5.8mmol/L.表示该体检指标的物理量是( )
| A、质量分数 | B、溶解度 |
| C、物质的量浓度 | D、摩尔质量 |
下列反应与Na2O2+SO2═Na2SO4相比较,Na2O2的作用相同的是( )
| A、2Na2O2+2CO2═2Na2CO3+O2↑ |
| B、2Na2O2+2SO3═2Na2SO4+O2↑ |
| C、Na2O2+H2SO4═Na2SO4+H2O2 |
| D、3Na2O2+Cr2O3═2Na2CrO4+Na2O |
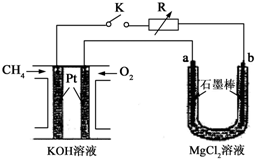 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.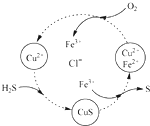 完成下列各小题的计算
完成下列各小题的计算