题目内容
16.某氢氧化钠溶液的实际浓度为0.1000mol/L.A同学的实验测定值为0.095mol/L,则他测定的相对误差为( )| A. | 5.26% | B. | -5.26% | C. | 5% | D. | -5% |
分析 相对误差的表达式为:$\frac{测定值-理论值}{理论值}$×100%,据此结合题中数据计算.
解答 解:该中和滴定的相对误差为:$\frac{0.095mol/L-0.1000mol/L}{0.1000mol/L}$×100%=-5%,
故选D.
点评 本题考查中和滴定的相关计算,题目难度不大,明确相对误差的含义即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
6.造成西安雾霾的重要原因之一是汽车尾气,已知汽车尾气无害化处理的反应之一为 2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0,下列说法正确的是( )
| A. | 升高温度可以提高NO和CO的转化率 | |
| B. | 使用高效催化剂可以提高NO和CO的转化率 | |
| C. | 反应达到平衡后,NO 的生成速率和消耗速率相等 | |
| D. | 若该反应已达到平衡状态,增大压强(通过减小体积实现)对平衡无影响 |
7.下列说法正确的是( )
| A. | 吸热反应一定需要加热才能发生 | |
| B. | 放热反应一定不需要加热就能进行 | |
| C. | 放热反应中,反应物的键能总和大于生成物的键能总和 | |
| D. | 吸热反应中,反应物的总能量小于生成物的总能量 |
4.下列措施不会影响水的电离平衡的是( )
| A. | 恒温条件下向水中加入少量Na2SO4固体 | |
| B. | 将水加热煮沸 | |
| C. | 恒温条件下向水中通入SO2气体 | |
| D. | 恒温条件下向水中通入氨气 |
11.在水溶液中显棕黄色的离子是( )
| A. | Fe3+ | B. | Fe2+ | C. | Cu2+ | D. | Al3+ |
7.在含有大量的Ba2+、OH-、Cl-的溶液中,还可能大量共存的离子是( )
| A. | CO32- | B. | NO3- | C. | H+ | D. | Fe3+ |
5.下列离子方程式的书写正确的是( )
| A. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| B. | 硫氢化钠水解:HS-+H2O??H3O++S2- | |
| C. | 硫化钾水解:S2-+H2O═HS-+OH- | |
| D. | 硫酸铝溶液跟偏铝酸钠溶液反应:Al3++3AlO2-+6H2O═4Al(OH)3↓ |
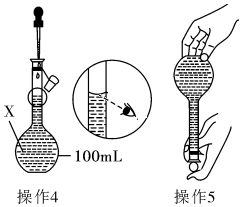 某同学欲配制100mL 0.10mol•L-1的CuSO4溶液.以下操作1~5是其配制的过程及示意图:
某同学欲配制100mL 0.10mol•L-1的CuSO4溶液.以下操作1~5是其配制的过程及示意图: