��Ŀ����
��14�֣�A��B��C��D��E��F�����ֶ���������Ԫ�أ����ǵ�ԭ������������������C��F�ֱ���ͬһ����Ԫ�أ�A��F����Ԫ�ص�ԭ�Ӻ���������֮�ͱ�C��D����Ԫ��ԭ�Ӻ���������֮����2��FԪ�ص������������Ǵ�����������0.75������֪BԪ�ص��������������ڲ��������2����EԪ�ص�������������������Ӳ�������ش�
��1��1 mol��E��F����Ԫ����ɵĻ��������A��C��D����Ԫ����ɵĻ����ﷴӦ���������κ�ˮ����ȫ��Ӧ�����ĺ��ߵ����ʵ���Ϊ ��
��2��A��C��F������γɼס������ָ�һ��˫ԭ�������ӣ�����18�����ӣ�����10�����ӣ�������ҷ�Ӧ�����ӷ���ʽΪ ��
��3����ѧ�о�֤������ѧ��Ӧ��ֻ��ʼ��̬�йأ�������ء�����B��ȼ����Ϊa kJ/mol����B��C����Ԫ����ɵĻ�����BC 14g��ȫȼ�շų�����b kJ��д������B�͵���C��Ӧ����BC���Ȼ�ѧ����ʽ
��
��4����ҵ���ڸ��µ������£�������A2C��BC��Ӧ��ȡ����A2���ڵ������I��II�����ܱ������зֱ����1 molA2C��1mol BC��2 mol A2C��2 mol BC��һ�������£���ַ�Ӧ��ֱ�ﵽƽ�⣨�������¶���ȣ�������˵����ȷ���� ��
A���ﵽƽ������Ҫ��ʱ�䣺I>II
B���ﵽƽ���A2C��ת���ʣ�I=II
C���ﵽƽ���BC�����ʵ�����I>II
D���ﵽƽ���A2�����������I<II
��5����BԪ�صĵ�����EԪ�صĵ��ʿ����Ƴɵ缫������A��C��D����Ԫ����ɻ�
�������Һ�й��ɵ�أ����ظ�����ӦʽΪ ��
��14�֣�
��1��8 mol��3�֣�
��2�� HS-+OH-=S2-+H2O��2�֣�
��3�� C��s��+ 1/2O2��g��=CO��g������H= -��a-2b�� kJ/mol��3�֣�
��4��A��B ��4�֣�
��5��2Al+8OH- -6e-=2AlO2-+4H2O��2�֣�
��������
���������FԪ�ص������������Ǵ�����������0.75������F�Ĵ�����������������2������FԪ����3����ӣ�������������8��������������6������F��SԪ�أ�C��F�ֱ���ͬһ����Ԫ�أ���C��OԪ�أ���֪BԪ�ص��������������ڲ��������2������B���ڲ��������������10����BԪ�ز�������3����ӣ������ڲ��������2����BԪ����CԪ�أ�EԪ�ص�������������������Ӳ�������E������H��Be��Al�����ǵ�ԭ������������������E��AlԪ�أ�A��F����Ԫ�ص�ԭ�Ӻ���������֮�ͱ�C��D����Ԫ��ԭ�Ӻ���������֮����2��DԪ��ֻ����F��Na��Mg��ѡ����D��F������OԪ�ص�������֮����17����AԪ�ز����ڣ���D��Na����A��HԪ�أ���D��Mg����A��He����������Ԫ�أ�����A��HԪ�أ�D��NaԪ�ء�
��1��1 mol��E��F����Ԫ����ɵĻ�����Al2S3����A��C��D����Ԫ����ɵĻ�����NaOH��Ӧ�����������Σ��������������ƺ�ƫ�����ƣ���Ӧ�Ļ�ѧ����ʽΪAl2S3+8NaOH=4H2O+2NaAlO2+3Na2S��������ȫ��Ӧ�������������Ƶ����ʵ���Ϊ8mol��
��2��A��C��F������γɼס������ָ�һ��˫ԭ�������ӣ�����18�����ӣ�����10�����ӣ������HS-������OH-�����߷�Ӧ���������Ӻ�ˮ�����ӷ���ʽ��HS-+OH-=S2-+H2O��
��3��1molC������ȫȼ�����ɶ�����̼�ų���������akJ���Ȼ�ѧ����ʽΪC��s��+ O2��g��=CO2��g������H= -a kJ/mol ��14gCO�����ʵ�����14g/28g/mol=0.5mol����1molCO��ȫȼ�����ɶ�����̼�ų���������2bkJ���Ȼ�ѧ����ʽ��CO��s��+ 1/2O2��g��=CO2��g������H= -2b kJ/mol��������ʽ�������C������������Ӧ����CO���Ȼ�ѧ����ʽ��ΪC��s��+ 1/2O2��g��=CO��g������H= -��a-2b�� kJ/mol��
��4����ҵ��ȡ�����Ļ�ѧ����ʽΪCO+ H2O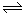 H2+CO2���÷�Ӧ���������ʵ�������Ŀ��淴Ӧ������I��II�ǵ�Чƽ�⡣A����ΪII�ķ�Ӧ���Ũ����I��2�������Է�Ӧ��Ũ������Ӧ���ʼӿ죬��ƽ���ʱ�䣺I>II����ȷ��B����Ϊͨ��ķ�Ӧ��ı�����ͬ�ģ����Դﵽ��ƽ���ǵ�Чƽ�⣬�ﵽƽ���A2C��ת���ʣ�I=II����ȷ��C���ﵽƽ���BC�����ʵ�����II��I��2��������D���ﵽƽ���A2�����������I=II������ѡAB��
H2+CO2���÷�Ӧ���������ʵ�������Ŀ��淴Ӧ������I��II�ǵ�Чƽ�⡣A����ΪII�ķ�Ӧ���Ũ����I��2�������Է�Ӧ��Ũ������Ӧ���ʼӿ죬��ƽ���ʱ�䣺I>II����ȷ��B����Ϊͨ��ķ�Ӧ��ı�����ͬ�ģ����Դﵽ��ƽ���ǵ�Чƽ�⣬�ﵽƽ���A2C��ת���ʣ�I=II����ȷ��C���ﵽƽ���BC�����ʵ�����II��I��2��������D���ﵽƽ���A2�����������I=II������ѡAB��
��5��C��Al��NaOH���ɵ�ԭ����У�Al��������ʧȥ�������������Ʒ�Ӧ����ƫ�����ƺ�ˮ�����Ը����ĵ缫��ӦʽΪ2Al+8OH- -6e-=2AlO2-+4H2O��
���㣺����Ԫ�ص��ƶϣ����ʵ��жϼ�����Ӧ�ã�����ʽ����д���绯ѧ��Ӧԭ����Ӧ��


 ��Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ
��Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ
 = ������Һ���������ӵ����ʵ���Ũ���ɴ�С��˳���� ��
= ������Һ���������ӵ����ʵ���Ũ���ɴ�С��˳���� ��