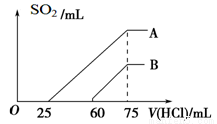
题目内容
(共14分)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。

已知W的一种原子的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z是同周期中非金属性最强的元素。
(1)Y位于元素周期表的位置 ,X与W元素形成的X2W2型化合物的电子式为
(2)Z的气态氢化物和溴化氢相比,较稳定的是 (写化学式)。
(3)Y与Z形成的化合物硬度小、熔点低、沸点低,其晶体中存在的作用力有
其分子属于 (填极性分子或非极性分子),它和足量水反应,有白色胶状沉淀产生,该反应的化学方程式是
(4)在25?C、101 kPa下,已知Y的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子,放热190.0kJ,该反应的热化学方程式是
(1)第三周期、ⅣA族 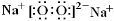 (2) HCl
(2) HCl
(3)范德华力(或分子间作用力);非极性分子;SiCl4+3H2O=H2SiO3↓+4HCl
或 SiCl4 +4H2O=H4SiO4↓+4HCl (4) SiH4(g)+2O2(g)=SiO2(s)+2H2O(l) ;△H=-1520.0kJ/mol
【解析】
试题解析:由信息及质子数+中子数=质量数,则W的质子数为18-10=8,则W为氧元素;由X和Ne原子的核外电子数相差1及X的原子半径比氧原子的半径大,则X为钠元素;Y的单质是一种常见的半导体材料,Y为短周期元素,则Y为硅元素;Z的电负性在同周期主族元素中最大及原子半径X>Y>Z,则Z为氯元素;(1)X为钠元素,位于周期表中第三周期第ⅠA族,X与W元素形成的X2W2型化合物的电子式为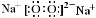 ;(2)因HCl中键长比HBr中键长短,键长越短越稳定,则HCl稳定;(3)Y与Z形成的化合物为SiCl4,它属于分子晶体,其晶体中存在的作用力有分子间的作用力(或范德华力),该分子的空间构型为正四面体型,它属于非极性分子,与足量水反应生成一种弱酸和一种强酸,由元素守恒可知应生成H2SiO3和HCl,反应为SiCl4+3H2O═H2SiO3↓+4HCll;(4)Y的气态氢化物为SiH4,在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,则1molSiH4燃烧转移8mol电子放热为190.0kJ×8=1520kJ,则该反应的热化学方程式为SiH4(g)+2O2(g)点燃SiO2(s)+2H2O△H=-1520kJ/mol。
;(2)因HCl中键长比HBr中键长短,键长越短越稳定,则HCl稳定;(3)Y与Z形成的化合物为SiCl4,它属于分子晶体,其晶体中存在的作用力有分子间的作用力(或范德华力),该分子的空间构型为正四面体型,它属于非极性分子,与足量水反应生成一种弱酸和一种强酸,由元素守恒可知应生成H2SiO3和HCl,反应为SiCl4+3H2O═H2SiO3↓+4HCll;(4)Y的气态氢化物为SiH4,在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,则1molSiH4燃烧转移8mol电子放热为190.0kJ×8=1520kJ,则该反应的热化学方程式为SiH4(g)+2O2(g)点燃SiO2(s)+2H2O△H=-1520kJ/mol。
考点:“位-构-性”的关系;化学键;热化学方程式


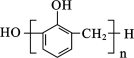
 它可以发生酯化、水解、加成等反应
它可以发生酯化、水解、加成等反应 O2(g)=2CO2(g)+H2O(g) ?△H=-1 256 kJ/mol
O2(g)=2CO2(g)+H2O(g) ?△H=-1 256 kJ/mol