题目内容
在一密闭容器中充入1mol H2和1mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)△H<0.
(1)保持容器容积不变,向其中加入1mol H2,反应速率 (加快、降低、不变).
(2)保持容器容积不变,向其中加入1mol N2,反应速率 (加快、降低、不变).
(3)保持容器内气体压强不变,向其中加入1mol N2,反应速率 (加快、降低、不变).
(4)保持容器内气体压强不变,向其中加入1mol H2(g)和1mol I2(g),反应速率 (加快、降低、不变).
(5)提高起始的反应温度,反应速率 (加快、降低、不变).
(1)保持容器容积不变,向其中加入1mol H2,反应速率
(2)保持容器容积不变,向其中加入1mol N2,反应速率
(3)保持容器内气体压强不变,向其中加入1mol N2,反应速率
(4)保持容器内气体压强不变,向其中加入1mol H2(g)和1mol I2(g),反应速率
(5)提高起始的反应温度,反应速率
考点:化学平衡的影响因素
专题:化学平衡专题
分析:在恒定温度下,反应速率的影响因素取决于浓度和压强,浓度越大,反应速率越大,如通入惰性气体,参加反应的物质的浓度不变,则反应速率不变,如压强不变,通入惰性气体,但体积增大,反应物的浓度减小,则反应速率减小,升高温度反应速率加快,以此解答该题.
解答:
解:(1)保持容器容积不变,向其中加入1molH2,反应物浓度增大,反应速率增大,故答案为:加快;
(2)保持容器容积不变,向其中加入1molN2,参加反应的物质的浓度不变,则反应速率不变,故答案为:不变;
(3)保持容器内气体压强不变,向其中加入1mol N2,体积增大,反应物的浓度减小,则反应速率减小,故答案为:降低;
(4)保持容器内气体压强不变,向其中加入1 mol H2(g)和1molI2(g),因体积增大为2倍,物质的量增大为2倍,则浓度不变,反应速率不变,故答案为:不变;
(5)升高温度反应速率加快,故答案为:加快.
(2)保持容器容积不变,向其中加入1molN2,参加反应的物质的浓度不变,则反应速率不变,故答案为:不变;
(3)保持容器内气体压强不变,向其中加入1mol N2,体积增大,反应物的浓度减小,则反应速率减小,故答案为:降低;
(4)保持容器内气体压强不变,向其中加入1 mol H2(g)和1molI2(g),因体积增大为2倍,物质的量增大为2倍,则浓度不变,反应速率不变,故答案为:不变;
(5)升高温度反应速率加快,故答案为:加快.
点评:本题考查化学反应速率,侧重于影响因素的考查,难度不大,注意把握影响因素,易错点为(2)和(3),注意惰性气体的特点.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
下列离子方程式中正确的是( )
| A、Al(OH)3滴加稀盐酸:OH-+H+=H2O |
| B、Fe片浸泡在FeCl3溶液中:Fe3++Fe=2Fe2+ |
| C、MgCl2溶液中滴加氨水:Mg2++2OH-=Mg(OH)2↓ |
| D、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
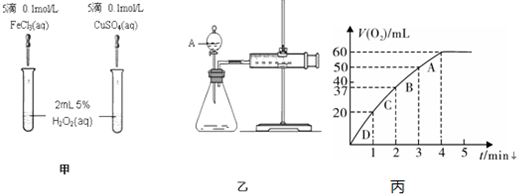


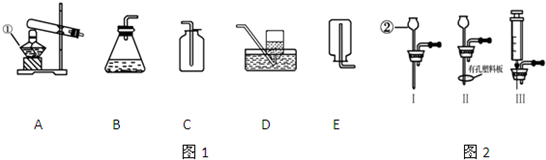
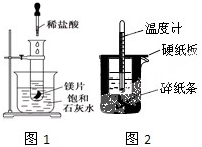 某学习小组设计以下实验,探究化学反应中的热效应.
某学习小组设计以下实验,探究化学反应中的热效应.