题目内容
已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白邑沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→自色沉淀,继续加入D溶液,白色沉淀逐渐消失。
(1)各物质分别是A ,B ,C 。
(2)i)写出②中反应的化学方程式: ,
。
ii)写出③中反应的离子方程式: ,
。
(1)BaCl2,FeSO4,AlCl3。(各1分)
(2)i)FeSO4+2NaOH=Fe(OH)2↓+Na2SO4(1分)
4Fe(OH)2+O2+2H2O=4Fe(OH)3(2分)
ii)Al3++3OH-=Al(OH)3↓(1分)
Al(OH)3+OH-=AlO2-+2H2O(a分)

练习册系列答案
相关题目
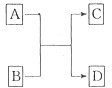
已知A、B、C、D分别是Cu、Ag、Fe、Al四种金属中的一种.已知①A、C均能与稀硫酸反应放出气体;②B与D的硝酸盐反应,置换出单质D;③C与强碱反应放出气体,由此可以推断A、B、C、D依次是( )
| A、Fe、Cu、Al、Ag | B、Al、Cu、Fe、Ag | C、Cu、Ag、Al、Fe | D、Ag、Al、Cu、Fe |
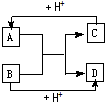 已知A、B、C、D分别是中学化学中常见的四种不同粒子,它们之间有如下图所示反应关系.
已知A、B、C、D分别是中学化学中常见的四种不同粒子,它们之间有如下图所示反应关系. 或
或
 (2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:
(2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题: →
→