题目内容
13.下列说法正确的是( )| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 金属单质在反应中只能作还原剂,非金属单质在反应中只能作氧化剂 | |
| C. | 氧化剂在反应中失去电子,还原剂在反应中得到电子 | |
| D. | 氧化剂具有氧化性,还原剂具有还原性 |
分析 A.处于中间价的微粒具有氧化性和还原性;
B.金属只能失去电子,而非金属可以得到或失去电子;
C.氧化剂得到电子,还原剂失去电子;
D.氧化剂得到电子,还原剂失去电子.
解答 解:A.处于中间价的微粒具有氧化性和还原性,如亚铁离子、亚硫酸根离子具有氧化性、还原性,故A错误;
B.金属只能失去电子,而非金属可以得到或失去电子,则金属单质在反应中只能作还原剂,非金属单质在反应中可作氧化剂或还原剂,故B错误;
C.氧化剂得到电子,还原剂失去电子,故C错误;
D.氧化剂得到电子,还原剂失去电子,则氧化剂具有氧化性,还原剂具有还原性,故D正确;
故选D..
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意从元素的化合价角度分析,题目难度不大.

练习册系列答案
相关题目
4.下列各组中的离子,能在溶液中大量共存的是( )
| A. | NO3-、Ag+、H+、Cl- | B. | CO32-、Na+、Ca2+、NO3- | ||
| C. | Mg2+、Cl-、OH-、CH3COO- | D. | Mg2+、SO42-、K+、Cl- |
1.设NA为阿伏加德罗常数的值,下列说法一定正确的是( )
| A. | 25℃,pH=13的NaOH溶液中含有OH-为0.1NA | |
| B. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| D. | 78 g Na2O2与足量的H2O反应,电子转移个数为2NA |
8.下列热化学方程式或离子方程式正确的是( )
| A. | 已知H2的标准燃烧热△H=-285.8 kJ•mol-1,则用热化学方程式可表示为:H2(g)+1/2O2(g)═H2O(g)△H=-285.8 kJ•mol-1 | |
| B. | 向NH4A1(SO4)2溶液中滴人Ba(OH)2溶液恰好使SO42-沉淀完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| C. | 已知中和热为57.3 kJ•mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH (aq)═Na2SO4 (aq)+2H2O ( l )△H=-114.6 kJ•mol-1 | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
18.在25mL碱式滴定管中盛放KOH溶液,将溶液的凹面调至“0”刻度后,再把其中的液体全部放出,则流出液体体积( )
| A. | 25mL | B. | 大于25mL | C. | 小于25mL | D. | 都不正确 |
5.下列物质中,既能与氢气在一定条件下加成,又能使酸性高锰酸钾溶液褪色,且属于芳香烃的是( )
| A. | 苯 | B. | 乙苯 | C. | 苯乙烯 | D. | 丁二烯 |
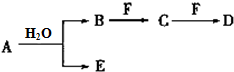 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.