题目内容
15.下面都是中学阶段几种常见的物质:A、Cu B、AgNO3溶液 C、H2SO4 D、NaOH E、过氧化钠 F、CO2 G、Al2(SO4)3 H、蔗糖,完成下列各题:(1)E的化学式为Na2O2,O的化合价为-1,颜色是淡黄色.
(2)属于非电解质的有F、H(填序号).
(3)写出G的电离方程式Al2(SO4)3═2Al3++SO42-.
(4)按要求写出下列反应的离子方程式:
①A+B:Cu+2Ag+═Cu2++2Ag.属于基本反应类型中的置换反应.
②C+D:H++OH-═H2O.反应类型为复分解反应.
(5)酸性氧化物是指与碱反应生成盐和水的氧化物,请写出上述物质中的酸性氧化物与碱反应的离子方程式:CO2+OH-═CO32-+H2O.
分析 (1)过氧化钠的化学式是Na2O2,为淡黄色固体,其中氧元素的化合价为-1价;
(2)在水溶液和熔融状态下都不导电的化合物属于非电解质;
(3)硫酸铝为强电解质,在溶液中完全电离出铝离子和硫酸根离子;
(4)铜与硝酸银溶液发生置换反应生成硝酸铜和银,硫酸与氢氧化钠发生中和反应生成硫酸钠和水,据此写出反应的离子方程式;
(5)各物质中酸性氧化物为二氧化碳,碱为氢氧化钠,二者反应生成碳酸钠和水.
解答 解:(1)过氧化钠中含有2个钠离子和1个过氧根离子,其化学式为:Na2O2,其中氧元素的化合价为-1价,过氧化钠为淡黄色固体,
故答案为:Na2O2;-1;淡黄色.
(2)非电解质是在水溶液和熔融状态下都不导电的化合物,满足条件的为:F、CO2、H、蔗糖,
故答案为:F、H;
(3)Al2(SO4)3在溶液中完全电离出铝离子和硫酸根离子,其电离方程式为:Al2(SO4)3═2Al3++SO42-,
故答案为:Al2(SO4)3═2Al3++SO42-;
(4)①铜与硝酸银溶液反应的离子方程式为:Cu+2Ag+═Cu2++2Ag,该反应为置换反应,
故答案为:Cu+2Ag+═Cu2++2Ag;置换;
②硫酸与氢氧化钠溶液反应的离子方程式为:H++OH-═H2O,该反应为属于复分解反应,
故答案为:H++OH-═H2O;复分解反应;
(5)上述各物质中,二氧化碳为酸性氧化物,氢氧化钠为碱,二者反应的离子方程式为:CO2+OH-═CO32-+H2O,
故答案为:CO2+OH-═CO32-+H2O.
点评 本题考查了离子方程式、电离方程式书写、电解质与非电解质的判断等知识,题目难度中等,试题知识点较多、综合性较强,充分考查了学生的灵活应用能力,注意掌握电离方程式、离子方程式的书写原则,明确电解质与非电解质的概念及判断方法.

| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 金属单质在反应中只能作还原剂,非金属单质在反应中只能作氧化剂 | |
| C. | 氧化剂在反应中失去电子,还原剂在反应中得到电子 | |
| D. | 氧化剂具有氧化性,还原剂具有还原性 |
| A. | 失去电子的是还原剂,表现氧化性 | |
| B. | 氧化还原反应的本质是元素化合价的升降 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 氧化还原反应中,某元素由化合物变为单质,此元素可能被还原,也可能被氧化 |
反应Fe(固)+H2O(气)?FeO(固)+H2(气)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
| 温度(绝对温度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(2)计算K值:温度为973开时K=0.618;1173开时:K=1.29.通过K值的计算(1)反应是吸热 反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2,在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
| 时间/min | CO2 | H2 | CO | H2O |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原因是升高温度或移走水蒸气.
| A. | 很多食物含有维生素,但蔬菜、水果比其他食物能提供更多的维生素 | |
| B. | 选择食物时,要考虑含营养素的种类、含量及是否易被人体吸收和利用 | |
| C. | 人体每天需要营养素的量是相对稳定的 | |
| D. | 三大热能食物中,糖类提供的热能最多,热值也最大 |
| 含杂质的物质 | 除杂试剂 | 有关离子方程式 |
| FeSO4(CuSO4) | ||
| Cu(Fe) | ||
| FeCl3(FeCl2) | ||
| FeCl2(FeCl3) |
| A. | 1molNaOH的摩尔质量为40g | |
| B. | 0.5molCO2约含有3.01×1023个CO2分子 | |
| C. | 1molN2的体积为22.4L | |
| D. | 1mol物质含有的微粒数就是6.02×1023 |
| A. | 将一小块Na投入CuSO4溶液中,生成蓝色沉淀,说明Cu比Na活泼 | |
| B. | 将带火星的木条放在Na2O2与H2O反应的试管口会复燃,说明反应生成了氧气 | |
| C. | 加热铝箔,铝箔熔化且失去光泽,但熔化的铝并不滴落,说明Al2O3的熔点高于Al | |
| D. | 将一小块Na投入水中,钠浮于水面,说明钠密度比水小 |
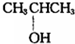 ⑨$\stackrel{13}{6}$C ⑩CH3OH.
⑨$\stackrel{13}{6}$C ⑩CH3OH.