题目内容
常温下,有关pH=3的醋酸溶液的说法正确的是( )
| A、醋酸溶液中,水的电离平衡向右移动 |
| B、加水稀释100倍后,溶液的pH=5 |
| C、加入CH3COONa固体,水的离子积常数Kw变小 |
| D、加入冰醋酸,醋酸的电离程度变小 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、酸电离出氢离子,会抑制水的电离;
B、加水稀释10n倍,弱酸的pH变化小于n个单位;
C、Kw只有温度有关;
D、醋酸的浓度越大,电离程度越小.
B、加水稀释10n倍,弱酸的pH变化小于n个单位;
C、Kw只有温度有关;
D、醋酸的浓度越大,电离程度越小.
解答:
解:A、酸电离出氢离子,会抑制水的电离,所以醋酸溶液中,水的电离平衡向左移动,故A错误;
B、加水稀释10n倍,弱酸的pH变化小于n个单位,则加水稀释100倍后,溶液的pH<5,故B错误;
C、Kw只有温度有关,温度不变,Kw不变,故C错误;
D、醋酸的浓度越大,电离程度越小,所以pH=3的醋酸溶液,加入冰醋酸,醋酸的浓度增大,其电离程度变小,故D正确.
故选D.
B、加水稀释10n倍,弱酸的pH变化小于n个单位,则加水稀释100倍后,溶液的pH<5,故B错误;
C、Kw只有温度有关,温度不变,Kw不变,故C错误;
D、醋酸的浓度越大,电离程度越小,所以pH=3的醋酸溶液,加入冰醋酸,醋酸的浓度增大,其电离程度变小,故D正确.
故选D.
点评:本题考查了弱电解质的电离、影响Kw的因素等,题目难度不大,侧重于基础知识的考查.

练习册系列答案
相关题目
常温时,将500mL pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法错误的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a) g CuCO3 |
| B、?b<a<7 |
| C、阳极电极反应:2H2O-4e-═O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |
下列各组混合物的分离或提纯方法不正确的是( )
| A、用过滤法分离Fe(OH)3胶体和FeCl3溶液的混合物 |
| B、用结晶法提纯NaCl和KNO3的混合物中的KNO3 |
| C、用蒸馏法分离乙醇和苯酚的混合物 |
| D、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
一定质量的A1、Mg合金与适量的稀硫酸恰好完全反应,将反应后的溶液蒸干,所得固体(不含结晶水)质量比原固体增加了4.8g,则该合金的物质的量可能为( )
| A、0.04mol |
| B、0.05mol |
| C、0.06mol |
| D、0.07mol |
已知:①C(s)+O2(g)=2CO2(g);?△H=393.5kJ/mol
②2CO(g)+O2(g)═2CO2(g);?△H=-566kJ/mol;
③TiO2(s)+2C2(g)═TiCl4(g)+O2(g);?H=+141kJ/mol 则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H为( )
②2CO(g)+O2(g)═2CO2(g);?△H=-566kJ/mol;
③TiO2(s)+2C2(g)═TiCl4(g)+O2(g);?H=+141kJ/mol 则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H为( )
| A、-313.5kJ/mol |
| B、+313.5kJ/mol |
| C、-80.0kJ/mol |
| D、+80.0kJ/mol |
联合国气候变化大会将于12月7日在丹麦哥本哈根召开,这次大会旨在达成一个真正全球性的、目标远大的(温室气体)减排协议.下列与此相关的叙述中,正确的是( )
| A、化学面对现代日益严重的环境问题显得越来越无能为力了 |
| B、化学是“污染”的代名词,一切污染皆因化学而起 |
| C、化学及分支学科面临着罕见的窘境,被人们淡忘、不重视是合乎情理的 |
| D、能源和环境问题的解决,过去、现在和将来都有赖于化学学科的发展 |
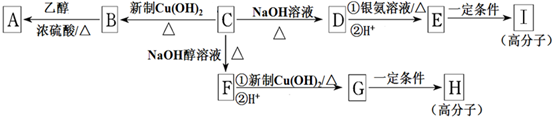
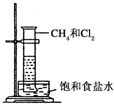 某课外兴趣小组利用如图装置探究甲烷与氯气的反应.根据题意,回答下列问题:
某课外兴趣小组利用如图装置探究甲烷与氯气的反应.根据题意,回答下列问题: