题目内容
室温时,下列混合溶液的pH一定小于7的是
A.pH=3的盐酸和pH=11的氨水等体积混合
B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合
C.pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合
D.pH=3的硫酸和pH=11的氨水等体积混合
C
【解析】
试题分析:A.盐酸是强酸,完全电离,pH=3的盐酸c(HCl)=c(H+)=10-3mol/L;一水合氨是弱碱,部分电离,溶液的pH=11,c(OH-)=10-3mol/L,所以c(NH3?H2O)> 10-3mol/L, 等体积混合时,NH3?H2O电离的部分恰好完全中和,过量的一水合氨会继续电离产生OH-,因此混合溶液的pH一定大于7,错误;B.盐酸是强酸,氢氧化钡是强碱,完全电离,所以pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合,二者恰好完全反应产生水,所以溶液的pH=7,错误;C.醋酸是弱酸,部分电离,氢氧化钡是强碱,完全电离,所以pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合,酸电离产生的H+与OH-恰好完全反应,未电离的酸分子会继续电离产生H+,因此混合溶液显酸性,pH<7,正确;D.硫酸是强酸,去电离,一水合氨是弱碱,部分电离,所以pH=3的硫酸和pH=11的氨水等体积混合,NH3?H2O电离的部分恰好完全中和,过量的一水合氨会继续电离产生OH-,因此混合溶液的pH一定大于7,错误。
考点:考查酸与碱溶液等体积混合时溶液酸碱性的计算的知识。

练习册系列答案
相关题目




 [Fe(SCN) ]2+ 。
[Fe(SCN) ]2+ 。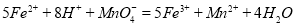 。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。