��Ŀ����
��8�֣�������Ѫ�쵰����Ҫ��ɳɷ֣�������������֯����O2�����ã����ȱ���Ϳ��ܳ���ȱ����ƶѪ�����������������Ҳ�к���������һ�ֳ�����ҩƷ˵�����еIJ������ݣ���ҩƷ��Fe2+33%��36%��������ˮ�������������е�θ���Vc��ά����C��ͬ�������ӱ�Ʒ���ա�
��һ����ͬѧ�����������ʵ����ò���ҩƷ���Ƿ���Fe2+��̽��Vc�����ã�

��1������������ˮ����Һ�з��������ӷ�Ӧ����ʽ��________________��Fe3+ +SCN-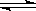 [Fe(SCN) ]2+ ��
[Fe(SCN) ]2+ ��
��2������KSCN��Һ����Һ��Ϊ����ɫ��˵����Һ��������Fe3+�������Ӵ��ڵ�ԭ������ǣ����ţ�_____________________��
A��ҩƷ�е���������Ӧ��������������ʽ����
B������ҩ��������������������
C��ҩƷ�������������������������
��3��ҩƷ˵�����С���Vcͬ�������ӱ�Ʒ���ա���˵������_______________________��
��������ͬѧ�����������������ø�����ر���Һ�ζ��ķ����ⶨ��ҩƷ�Ƿ�ϸ�Ӧԭ��Ϊ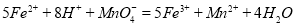 ��ȷ��������ҩƷ10.00g������ȫ�������Լ�2�У��� �Ƴ�1000mL��Һ��ȡ��20.00mL����0.0200mol/L��KMnO4��Һ�ζ�����ȥKMnO4��Һ12.00mL��
��ȷ��������ҩƷ10.00g������ȫ�������Լ�2�У��� �Ƴ�1000mL��Һ��ȡ��20.00mL����0.0200mol/L��KMnO4��Һ�ζ�����ȥKMnO4��Һ12.00mL��
��4����ʵ���е��Լ�2���ͬѧ��Ƶ�ʵ���е��Լ�1��������______������ţ���
A������ˮ B��ϡ���� C��ϡ���� D��ϡ����
��5����ʵ��ζ������в����ζ��ܵ�ͼʾ��ȷ����_______�����ţ���

��6����ͨ�����㣬˵����ҩƷ�����������Ƿ�ϸ�д����Ҫ������̣���
��1��2Fe2++Cl2=2Fe3++2Cl-����2��B��C
��3��Fe2+������Ѫ�쵰��������O2�����ã�Fe3+û�д˹��ܣ�����Vc�ɷ�ֹҩƷ�е�Fe2+��������Fe3+���������ֻ������Fe2+��Fe2+������Ѫ�쵰��������O2�����ã�����Vc�ɷ�ֹҩƷ�е�Fe2+��������Fe3+��������������Ҳ�ɸ��֣�����4��C��5��A
��6��33.6%���ϸ�
��������
�����������1��������ˮ�к��д������������ӣ�����Fe2+����ΪFe3+������������ˮ����Һ�з��������ӷ�Ӧ����ʽ��2Fe2++Cl2=2Fe3++2Cl-��Fe3+ +SCN- [Fe(SCN) ]2+ ����2������KSCN��Һ����Һ��Ϊ����ɫ��˵����Һ��������Fe3+��ԭ������ǣ�A��ҩƷ�е���������Ӧ���Զ���������ʽ���ڣ�����B������ҩ�����в���Fe2+����������������������������ȷ��C��ҩƷ��������в���Fe2+���������������������������ɣ���ȷ����ѡ����B��C; ��3��ҩƷ˵�����С���Vcͬ�������ӱ�Ʒ���ա�ԭ����Vc�л�ԭ�ԣ���Ѳ��ֱ���ΪFe3+��ԭΪFe2+���Ӷ���ǿFe2+������Ѫ�쵰��������O2�����ã�Fe3+û�д˹��ܡ���4���ڵڶ��ַ����ⶨFe2+�ĺ���ʱҪ���ữ�ĸ��������Һ���������᱾���������ԣ�����ʹ�ã������л�ԭ��Ҳ�ᷴӦ���ĸ�����أ��Dzⶨ�����ȷ�������ữ��ҺӦ��ʹ�����ᣬ��˸�ʵ���е��Լ�2���ͬѧ��Ƶ�ʵ���е��Լ�1�����������ᣬѡ����C����5����ʵ��ζ������в����ζ��ܵ�ͼʾ��ȷ����A����6��n(MnO4-)=0.0200mol/L ��0.012L��(1000mL��20ml) = 0.0120mol�����ݷ�Ӧ����ʽ��֪n(Fe2+)=5 n(MnO4-)=0.012mol��5=0.0600mol; m(Fe2+)=0.0600mol�� 56g/mol=3.36g������Fe2+�ĺ����ǣ�3.36g ��10.00g����100%=33.6%����33%��36%��Χ�ڣ���˸�ҩƷ�Ǻϸ�ġ�
[Fe(SCN) ]2+ ����2������KSCN��Һ����Һ��Ϊ����ɫ��˵����Һ��������Fe3+��ԭ������ǣ�A��ҩƷ�е���������Ӧ���Զ���������ʽ���ڣ�����B������ҩ�����в���Fe2+����������������������������ȷ��C��ҩƷ��������в���Fe2+���������������������������ɣ���ȷ����ѡ����B��C; ��3��ҩƷ˵�����С���Vcͬ�������ӱ�Ʒ���ա�ԭ����Vc�л�ԭ�ԣ���Ѳ��ֱ���ΪFe3+��ԭΪFe2+���Ӷ���ǿFe2+������Ѫ�쵰��������O2�����ã�Fe3+û�д˹��ܡ���4���ڵڶ��ַ����ⶨFe2+�ĺ���ʱҪ���ữ�ĸ��������Һ���������᱾���������ԣ�����ʹ�ã������л�ԭ��Ҳ�ᷴӦ���ĸ�����أ��Dzⶨ�����ȷ�������ữ��ҺӦ��ʹ�����ᣬ��˸�ʵ���е��Լ�2���ͬѧ��Ƶ�ʵ���е��Լ�1�����������ᣬѡ����C����5����ʵ��ζ������в����ζ��ܵ�ͼʾ��ȷ����A����6��n(MnO4-)=0.0200mol/L ��0.012L��(1000mL��20ml) = 0.0120mol�����ݷ�Ӧ����ʽ��֪n(Fe2+)=5 n(MnO4-)=0.012mol��5=0.0600mol; m(Fe2+)=0.0600mol�� 56g/mol=3.36g������Fe2+�ĺ����ǣ�3.36g ��10.00g����100%=33.6%����33%��36%��Χ�ڣ���˸�ҩƷ�Ǻϸ�ġ�
���㣺�������ӷ���ʽ����д�����ʵļ��鷽�������ڻ�ѧ����ʽ�ļ��㡢�������ʺ����ļ����֪ʶ��

����ʵ�鲻�ܴﵽԤ��ʵ��Ŀ�ĵ���( )
��� | ʵ������ | ʵ��Ŀ�� |
A | ��2.5gCuSO4��5H2O�ܽ���97.5gˮ�� | ������������Ϊ1.6����CuSO4��Һ |
B | ��ʢ��1mL��������Һ���Թ��еμ�NaCl��Һ���������г������ɣ��������еμ�Na2S��Һ | ˵��һ�ֳ�����ת��Ϊ��һ���ܽ�ȸ�С�ij��� |
C | �����£���pH��ֽ�ⶨŨ��Ϊ0.1mol��L��1NaClO��Һ��0.1mol��L��1CH3COONa��Һ��pH | �Ƚ�HClO��CH3COOH������ǿ�� |
D | �����£��ֱ���2֧�Թ��м�����ͬ�������ͬŨ�ȵ�Na2S2O3��Һ���ٷֱ������ͬ�����ͬŨ�ȵ�ϡ���� | �о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
 2Z(g)�ﵽƽ��ʱ�����Y��ת����Ϊ37��5%��X��ת����Ϊ25%����Ӧ��ʼʱ�����������е�X��Y�����ʵ���֮���ǣ�
2Z(g)�ﵽƽ��ʱ�����Y��ת����Ϊ37��5%��X��ת����Ϊ25%����Ӧ��ʼʱ�����������е�X��Y�����ʵ���֮���ǣ� 2CO��g���SH=+QkJ��mol���ﵽƽ��״̬���ֽ������²����������߷�Ӧ��ϵ���¶ȣ������ӷ�Ӧ��C������������С��Ӧ��ϵ��������ܼ�����ϵ��CO������������ʩ��һ����ʹ��Ӧ������Ӧ���������ӿ�� �� ��
2CO��g���SH=+QkJ��mol���ﵽƽ��״̬���ֽ������²����������߷�Ӧ��ϵ���¶ȣ������ӷ�Ӧ��C������������С��Ӧ��ϵ��������ܼ�����ϵ��CO������������ʩ��һ����ʹ��Ӧ������Ӧ���������ӿ�� �� ��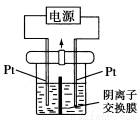
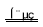 KIO3��3H2��
KIO3��3H2��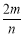 B��
B��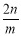 C��
C��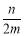 D��
D��