题目内容
20.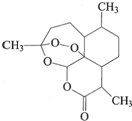 中国药学家屠呦呦获得2015年诺贝尔生理医学奖.她发现了青蒿素--一种用于治疗疟疾的药物,挽救了全球数百万人的生命.青蒿素的结构如图所示.下列有关青蒿素的说法不正确的是( )
中国药学家屠呦呦获得2015年诺贝尔生理医学奖.她发现了青蒿素--一种用于治疗疟疾的药物,挽救了全球数百万人的生命.青蒿素的结构如图所示.下列有关青蒿素的说法不正确的是( )| A. | 分子式为C15H22O5 | |
| B. | 易溶于乙醚等有机溶剂 | |
| C. | 可发生取代反应,不能发生氧化反应 | |
| D. | 在强酸或强碱性溶液中不能稳定存在 |
分析 可根据有机物的结构简式判断分子式为C15H22O5,分子中含有-O-O-键,具有强氧化性,含有-COO-,可发生水解反应,含有较多憎水基,难溶于水.
解答 解:A.根据有机物的结构简式判断分子式为C15H22O5,故A正确;
B.该有机物含有醚键,与乙醚相似相溶,易溶于乙醚,故B正确;
C.分子中含有过氧键,具有较强的氧化性,故C错误;
D.含有-COO-,可在酸性、碱性条件下发生水解,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意把握有机物官能团的结构和性质.

练习册系列答案
相关题目
10. 自然界中存在大量的金属元素,其 中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其 中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
则A原子的价电子排布式为3s2.
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N;
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4;
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
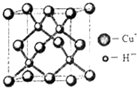
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
 自然界中存在大量的金属元素,其 中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其 中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N;
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4;
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
8.硫酸性质是中学化学学习的重点.请回答下列问题:
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:乙烯(写一种).
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验.
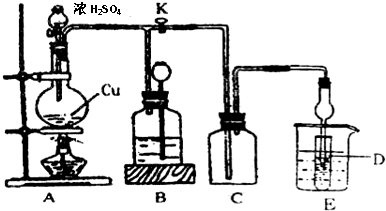
①装置B的作用是贮存多余的气体.B中应放置的液体是d(填序号).
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是b(填序号).
a.Fe粉b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是2Cu+2H2SO4+O2=2CuSO4+2H2O.
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是Ⅲ(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为Cl2+SO2+2H2O=4H++2Cl-+SO42-.D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=2 c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(3)利用FeCl3溶液的氧化性也可以吸收SO2.
①该反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.检验FeCl3是否完全被还原的方法为取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原.
②为验证FeCl3溶液与SO2的反应:同学们将SO2通入0.05mol•L-1 FeCl3溶液中,溶液很快由黄色变为红褐色; 将溶液长时间放置后,最终变为浅绿色. 关于红褐色液体,以下是同学们的分析推测及实验.
利用胶体的丁达尔效应(填性质) 可以检验步骤ⅰ中是否得到了Fe(OH) 3胶体.
根据反应b,说明步骤ⅱ中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应Fe3++6SO2?Fe(SO2)63+ 逆向移动(用离子方程式结合必要的文字说明).
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:乙烯(写一种).
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验.

①装置B的作用是贮存多余的气体.B中应放置的液体是d(填序号).
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是b(填序号).
a.Fe粉b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是2Cu+2H2SO4+O2=2CuSO4+2H2O.
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是Ⅲ(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为Cl2+SO2+2H2O=4H++2Cl-+SO42-.D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=2 c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(3)利用FeCl3溶液的氧化性也可以吸收SO2.
①该反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.检验FeCl3是否完全被还原的方法为取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原.
②为验证FeCl3溶液与SO2的反应:同学们将SO2通入0.05mol•L-1 FeCl3溶液中,溶液很快由黄色变为红褐色; 将溶液长时间放置后,最终变为浅绿色. 关于红褐色液体,以下是同学们的分析推测及实验.
| 分析推测 | 实验步骤及现象 |
| 甲:生成了Fe(OH) 3胶体 乙:经查阅资料,可能发生反应:Fe3++6SO2?Fe(SO2)63+ (反应b) | ⅰ.制备Fe(OH) 3胶体并检验 ⅱ.分别向Fe(OH) 3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
根据反应b,说明步骤ⅱ中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应Fe3++6SO2?Fe(SO2)63+ 逆向移动(用离子方程式结合必要的文字说明).
15.关于电化学内容,下列说法正确的是( )
| A. | 氢氧燃料电池的负极反应式:O2+4H++4e-═2H2O | |
| B. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| C. | 粗铜精炼时,与电源正极相连是纯铜,电极反应式为Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
12.下列现象不能用氢键解释的是( )
| A. | 冰的密度小于液态水 | B. | 氨气易液化 | ||
| C. | HF的沸点高于HI | D. | 有机物普遍存在同分异构现象 |
10.下列说法正确的是(设NA为阿伏伽德罗常数)
| A. | 标准状况下,2.24LSO3中硫原子数与1L0.1mol•L-1Na2SO3溶液中硫原子数相同 | |
| B. | 1mol•L-1FeCl3溶液全部制成胶体,其中含胶粒的数目小于NA | |
| C. | 1molNa2O2中含有NA个阴离子 | |
| D. | 1L0.5mol•L-1Na2SO4溶液中阴离子所带电荷数为NA |