题目内容
C、N、O三种元素第一电离能从大到小的顺序是 .
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素.
解答:
解:C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C,
故答案为:N>O>C.
故答案为:N>O>C.
点评:本题考查了第一电离能大小比较,把握同周期元素的第一电离能变化规律即可解答,题目难度不大.

练习册系列答案
相关题目
当光束通过豆浆时,可观察到丁达尔效应,表明豆浆是胶体,胶体区别于其它分散系的本质特征是( )
| A、丁达尔现象 |
| B、胶体粒子能透过滤纸 |
| C、外观均一、均一、稳定、透明 |
| D、分散质粒子的直径在1~100 nm之间 |

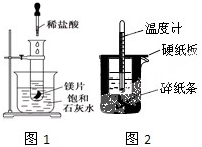 某学习小组设计以下实验,探究化学反应中的热效应.
某学习小组设计以下实验,探究化学反应中的热效应.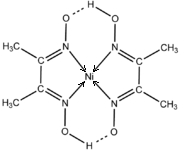 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.