题目内容
8.下列说法不正确的是( )| A. | Na2CO3溶液中c(Na+)与c(CO32-)之比大于2:1 | |
| B. | 蒸发氯化铝溶液要不断通入氯化氢气体方可得到氯化铝晶体 | |
| C. | 1 L 0.3 mol/L醋酸溶液中H+个数与3 L 0.1 mol/L醋酸溶液中H+个数之比为1:1 | |
| D. | 浓度相同的下列溶液中,按pH由小到大的顺序排列的是CH3COONa、NaHCO3、Na2CO3 |
分析 A.CO32-发生水解;
B.氯化铝溶液加热时易发生水解,通入氯化氢可抑制水解;
C.醋酸浓度越大,电离程度越小;
D.盐对应的酸越弱,水解程度越大.
解答 解:A.碳酸钠为强碱若酸盐,CO32-发生水解,则Na2CO3溶液中c(Na+)与c(CO32-)之比大于2:1,故A正确;
B.氯化铝溶液加热时易发生水解生成氢氧化铝和HCl,通入氯化氢可抑制水解,故B正确;
C.醋酸浓度越大,电离程度越小,则1 L 0.3 mol/L醋酸溶液中H+个数与3 L 0.1 mol/L醋酸溶液中H+个数之比小于1:1,故C错误;
D.CO32-以第一步水解为主,且盐对应的酸越弱,水解程度越大,则浓度相同的下列溶液中,按pH由小到大的顺序排列的是CH3COONa、NaHCO3、Na2CO3,故D正确.
故选C.
点评 本题考查较为综合,涉及多方面的知识,为高频考点和常见题型,注意把握盐类水解的原理、影响因素以及应用,难度不大.

练习册系列答案
相关题目
18.某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物
测定生成气体的体积
方案Ⅱ:铜铝混合物
测定剩余固体的质量
下列有关判断中不正确的是( )
方案Ⅰ:铜铝混合物
| 足量溶液A |
| 充分反应 |
方案Ⅱ:铜铝混合物
| 足量溶液B |
| 充分反应 |
下列有关判断中不正确的是( )
| A. | 溶液A和B均可以是盐酸 | B. | 溶液A和B均可以是NaOH溶液 | ||
| C. | 溶液A和B均可选用稀硝酸 | D. | 实验室中方案Ⅱ更便于实施 |
19.A、B、C、D、E为原子序数依次增大的短周期元素,其中只有一种是金属元素.A、D元素原子最外层电子数相同,且A和D可形成离子化合物,C2-和D+具有相同的电子数,E元素的最高正化合价与最低负化合价之和为2.由这些元素组成的物质,其组成和结构信息如下表:
请用化学用语回答下列问题:
(1)D+的结构示意图为 ;
;
(2)C、D、E的氢化物按熔点由高到低排列的顺序为NaH>H2O>PH3;
(3)乙属于极性分子(填“极性”或“非极性”),丁的电子式为 ,
,
(4)将少量甲投入到AlCl3溶液中反应的离子方程式为6Na2O2+4Al3+6H2O=4Al(OH)3↓+3O2↑+12Na+;
(5)氮化硼晶体的熔点要比丙晶体高,其原因是磷原子半径比氮原子大,N-B共价键键长比B-P小,则N-B键能大.
| 物质 | 组成和结构信息 |
| 甲 | 含有非极性共价键的常见二元离子化合物 |
| 乙 | 含有极性键和非极性键的18e-分子 |
| 丙 | 化学组成为BE,熔点高,可作超硬耐磨涂层材料 |
| 丁 | 化学组成为DBA4的离子化合物 |
(1)D+的结构示意图为
 ;
;(2)C、D、E的氢化物按熔点由高到低排列的顺序为NaH>H2O>PH3;
(3)乙属于极性分子(填“极性”或“非极性”),丁的电子式为
 ,
,(4)将少量甲投入到AlCl3溶液中反应的离子方程式为6Na2O2+4Al3+6H2O=4Al(OH)3↓+3O2↑+12Na+;
(5)氮化硼晶体的熔点要比丙晶体高,其原因是磷原子半径比氮原子大,N-B共价键键长比B-P小,则N-B键能大.
16.在NaClO中加入浓盐酸产生黄绿色气体X,在Na2SO3中加入稀H2SO4产生无色气体Y,下列对X、Y的叙述中错误的是( )
| A. | 将X、Y分别通入品红溶液中,均使品红溶液褪色 | |
| B. | 将X、Y分别通入氢硫酸中,只有Y能产生沉淀 | |
| C. | 等物质的量的X、Y同时通入品红溶液中,品红溶液不褪色 | |
| D. | 等物质的量的X、Y同时通入BaCl2溶液中,有沉淀产生 |
3.用pH传感器测得0.10mol•L-1Na2CO3溶液从55℃升高至85℃的pH如图所示.在55℃升高至85℃升温过程中,下列说法正确的是( )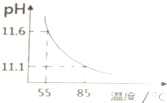

| A. | c(H+)增大,c(OH-)减小 | B. | $\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})}$比值不断增大 | ||
| C. | c(CO32-)+c(HCO3-)+c(H2CO3)=0.10 | D. | c(OH-)-c(HCO3-)-c(H2CO3)=10-11.1 |
13.常温下,将a1mLb1mol•L-1CH3COOH溶液加入到a2mLb2mol•L-1NaOH溶液.下列结论中正确的是( )
| A. | 若a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| B. | 若a1=a2,b1=2b2,则混合溶液中c(CH3COO-)>c(CH3COOH)>c(Na+) | |
| C. | 若a1b1>a2b2,则混合液的pH一定大于7 | |
| D. | a1=a2,且混合溶液的pH<7,则b1一定大于b2 |
20.下列物质的水溶液只存在溶质分子的是( )
| A. | HCl | B. | CH3COOH | C. | 蔗糖 | D. | Na2CO3 |
17.某烷烃的相对分子质量为114,与氯气发生取代反应所得的一氯代物只有一种的是( )
| A. | CH3CH3 | |
| B. |  | |
| C. |  | |
| D. | CH3CH2CH2CH3 |
3.常温下,稀释0.1mol•L-1Na2CO3溶液,图中的纵坐标可以表示( )


| A. | 溶液中HCO3-的数目 | B. | 溶液的pH | ||
| C. | CO32- 水解的平衡常数 | D. | 溶液中的c(CO32-) |