题目内容
4.2A(g)?2B(g)+C(g);△H>0,达平衡时,要使v正降低、c(A)增大,应采取( )| A. | 加压 | B. | 减压 | C. | 减少A | D. | 降温 |
分析 达平衡时,要使v正降低,可采取降低温度、减小压强或减小浓度的措施,使c(A)增大,应使平衡向逆反应方向移动,
解答 解:A.增大压强,反应速率增大,故A错误;
B.减小压强,平衡正向移动,c(A)减小,故B错误;
C.减小A的浓度,平衡逆向移动,平衡移动的结果是减弱,而不是抵消,所以平衡时c(A)减小,故C错误;
D.降温,反应速率减小,平衡逆向移动,c(A)增大,故D正确.
故选D.
点评 本题考查外界条件对化学平衡的影响,为高频考点,侧重于学生的分析能力的考查,难度不大,本题注意根据反应方程式的特征判断平衡移动的方向.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的体积扩大两倍,测得A的浓度变为0.35mol/L,下列有关判断正确的是( )
| A. | x+y<z | B. | 平衡正向移动 | C. | B的浓度增大 | D. | A的转化率降低 |
8.关于阿斯匹林的作用叙述中不正确的是( )
| A. | 杀菌消炎 | B. | 解热镇痛 | C. | 防止心脏病发作 | D. | 提高免疫力 |
5.用 NA 表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | T℃1 L pH=6 的纯水中含 10-6 NA个 OH | |
| B. | 6.0 g SiO2 晶体中含有 0.1 NA 个 SiO2分子 | |
| C. | 标准状况下,22.4 L HF 所含电子数为 10NA | |
| D. | 标准状况下,22.4 L 氧气作氧化剂时转移电子数一定为 4NA |
12.关于有机物 的说法不正确的是( )
的说法不正确的是( )
 的说法不正确的是( )
的说法不正确的是( )| A. | 能与溴水发生加成反应 | B. | 分子中所有的碳原子在同一平面上 | ||
| C. | 能与碳酸氢钠发生反应 | D. | 能发生取代、氧化反应 |
9.下列离子方程式中,正确的是( )
| A. | 向NaOH溶液中加入少量Mg(HCO3)2溶液:2OH-+Mg2+═Mg(OH)2↓ | |
| B. | 向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:2HCO3-+Ba2++2H++SO42-═BaSO4↓+2H2O+2CO2↑ | |
| C. | 酸性KMnO4溶液与H2O2反应:2MnO4-+10H++3H2O2═2Mn2++3O2↑+8H2O | |
| D. | 向Fe(NO3)3溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 |
13.下列化学用语表示正确的是( )
| A. | 氯气的电子式:Cl:Cl | |
| B. | 乙烯的结构简式CH2CH2 | |
| C. | 钠原子的结构示意图: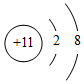 | |
| D. | 硫酸亚铁的电离方程式FeSO4═Fe2++SO42- |
14.在如图实验中,下列说法错误的是( )
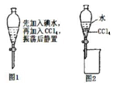

| A. | 从碘水中提取单质碘时,不能用无水乙醇代替四氯化碳 | |
| B. | 进行如图1操作后,实验现象为液体分层,下层呈无色 | |
| C. | 利用如图2装置可以分离四氯化碳和水 | |
| D. | 在这个操作中,应选择有机萃取剂,且萃取剂不溶于水 |



