题目内容
氯气是一种重要的化工原料.某学习小组在实验室中利用下图装置制取氯气并探究其性质.

(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有 ;
(2)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
(3)证明FeBr2与Cl2发生了氧化还原反应的实验方法是 (填操作方法).

(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
(2)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
(3)证明FeBr2与Cl2发生了氧化还原反应的实验方法是
考点:氯气的化学性质
专题:卤族元素
分析:(1)二氧化锰和浓盐酸反应制取氯气加热需酒精灯,需要用分液漏斗加浓盐酸;
(2)氯气具有强氧化性,能够溴化亚铁中的溴离子和二价铁离子,生成单质溴和三价铁离子;
(3)三价铁离子和硫氰酸钾溶液反应生成血红色溶液;生成的溴单质可以利用四氯化碳萃取的现象来分析发生了反应.
(2)氯气具有强氧化性,能够溴化亚铁中的溴离子和二价铁离子,生成单质溴和三价铁离子;
(3)三价铁离子和硫氰酸钾溶液反应生成血红色溶液;生成的溴单质可以利用四氯化碳萃取的现象来分析发生了反应.
解答:
解:(1)二氧化锰和浓盐酸反应制取氯气的方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,该反应需加热,所以需酒精灯;反应物浓盐酸的滴加以及防氯气的逸出需要用分液漏斗,
故答案为:分液漏斗、酒精灯;
(2)D中品红溶液褪色,B中通入足量的氯气,氯气具有强氧化性,足量的氯气与溴化亚铁反应生成氯化铁和溴,离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2,
故答案为:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2;
(3)要证明FeBr2与Cl2发生了氧化还原反应,只需分别证明三价铁离子和溴单质的存在,而三价铁离子和硫氰酸钾溶液反应生成血红色溶液,溴的四氯化碳显棕红色,所以操作方法为:取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取;
故答案为:取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取.
| ||
故答案为:分液漏斗、酒精灯;
(2)D中品红溶液褪色,B中通入足量的氯气,氯气具有强氧化性,足量的氯气与溴化亚铁反应生成氯化铁和溴,离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2,
故答案为:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2;
(3)要证明FeBr2与Cl2发生了氧化还原反应,只需分别证明三价铁离子和溴单质的存在,而三价铁离子和硫氰酸钾溶液反应生成血红色溶液,溴的四氯化碳显棕红色,所以操作方法为:取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取;
故答案为:取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取.
点评:本题考查了氯气的实验室制备和性质,解题关键在于理解制取的原理和熟悉氯气的化学性质,题目难度不大.

练习册系列答案
相关题目
含有0.30g甲醛的水溶液与过量银氨溶液充分反应,生成的银有( )
| A、0.02g |
| B、0.04g |
| C、2.16g |
| D、4.32g |
下列属于同分异构体的组合是( )
| A、戊烷与乙烷 |
| B、淀粉和纤维素 |
C、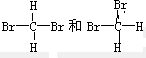 |
| D、CH3CH2CH2CH3和CH3CH(CH3)2 |
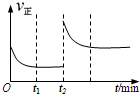 一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=
一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=