题目内容
20.铝在空气中能够稳定存在的原因是( )| A. | 铝的性质不活泼 | B. | 铝的还原性弱 | C. | 铝与氧气不反应 | D. | 铝表面有氧化膜 |
分析 金属铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止了铝进一步氧化,使铝在空气中能够稳定存在.
解答 解:A.金属铝是一种比较活泼的金属,故A错误;
B.铝的活泼性较强,易失去电子,具有较强的还原性,故B错误;
C.常温下,铝在空气中与氧气反应生成氧化铝,故C错误;
D.铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,这是铝在空气中能够稳定存在的原因,故D正确;
故选D.
点评 本题主要考查了铝的化学性质,题目难度不大,明确常见元素及其化合物性质为解答关键,注意铝在空气中能够稳定存在,不是铝不活泼,而是生成的一层致密的氧化物薄膜.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
1.在25℃的纯水中,水的离子积(KW)为( )
| A. | KW=1×10-14 | B. | 大于1×10-14 | C. | 小于1×10-14 | D. | 0.01 |
8.用玻璃棒蘸浓硫酸滴在纸上,纸变黑,这表现了浓硫酸的( )
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 |
15.下列各种高聚物中,具有热固性的是( )
| A. | 聚乙烯 | B. | 聚氯乙烯 | C. | 聚丙烯 | D. | 酚醛塑料 |
5.下列装置能达到实验目的是( )
| A. | 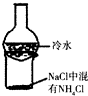 加热烧杯,可用来分离NaCl和NH4Cl | B. | 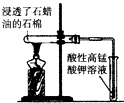 石蜡油分解实验 | ||
| C. |  比较MnO2、Cl2、S的氧化性 | D. | 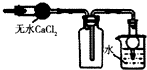 收集干燥的氨气 |
12.下列实验符合“绿色环保”思想的是( )
| A. |  制氯水 | B. |  铜与浓硫酸反应 | ||
| C. | 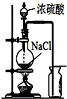 制氯化氢气体 | D. |  一氧化碳还原氧化铜 |
10.在反应中,既能放出气体,又不是氧化还原反应的是( )
| A. | Na和水反应 | B. | Na2O2和水反应 | ||
| C. | 氯化铵与氢氧化钙反应 | D. | MnO2与浓盐酸共热 |