题目内容
19.命名下列有机物(1)
 2,3-二甲基-2-戊烯
2,3-二甲基-2-戊烯(2)
 2-丁醇
2-丁醇(3)
 二乙酸乙二醇酯
二乙酸乙二醇酯(4)
 1,2,4-三甲基苯.
1,2,4-三甲基苯.
分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:(1)从距离官能团近的一端命名,命名为:2,3-二甲基-2-戊烯,故答案为:2,3-二甲基-2-戊烯;
(2)选择包含羟基的最长碳连为主链,命名为:2-丁醇,故答案为:2-丁醇;
(3)酯的命名为某酸某酯,命名为:二乙酸乙二醇酯,故答案为:二乙酸乙二醇酯;
(4)取代基的位次和最小,命名为:1,2,4-三甲基苯,故答案为:1,2,4-三甲基苯.
点评 本题考查了有机物系统命名方法的应用,注意主链选择,起点编号原则,名称书写的规范方法,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列图示实验正确的是( )
| A. | 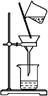 除去粗盐溶液中的不溶物 | B. |  碳酸氢钠受热分解 | ||
| C. | 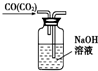 除去CO气体中的CO2气体 | D. | 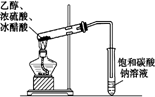 乙酸乙酯制备演示实验 |
10.
I:(1)第三周期元素M的电离能情况如甲图A所示.则M元素的价层电子排布式是3s2
(2)图B折线c(选填“a”、“b”或“c”)可以表达出第ⅣA族元素氢化物的沸点的变化规律.其中点A表示的分子的化学式为H2O,其沸点较高是因为水分子间可以形成氢键.
(3)COCl2 俗称光气,分子中C原子采取sp2杂化成键;其中分子中的共价键含有C(填序号):
A 2个σ键 1个π键 B 2个键π C 3个σ键、1个π键
Ⅱ:海水中富含氯元素.
(4)KCl广泛应用于医药和农业,KCl晶体中基态的Cl-电子排布式为1s22s22p63s23p6
(5)下列是IA族的Li、Na、K三种金属元素的电离能
则三种金属的氯化物(RCl)的熔点由高到低的顺序为LiCl>NaCl>KCl(用化学式回答),原因是随核电荷数增大,阳离子半径增大,晶格能减小,熔点降低
(6)RCl用作有机机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图乙所示.R的元素符号是Cu,每个Cl-周围最近的Cl-12个.已知该晶体密度为1.15 g/cm3,则晶胞中最近的R+和Cl-之间的距离为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{4×99.5}{1.15×6.02×1{0}^{23}}}$cm(NA=6.02×1023/mol,只写出计算表达式即可)

I:(1)第三周期元素M的电离能情况如甲图A所示.则M元素的价层电子排布式是3s2
(2)图B折线c(选填“a”、“b”或“c”)可以表达出第ⅣA族元素氢化物的沸点的变化规律.其中点A表示的分子的化学式为H2O,其沸点较高是因为水分子间可以形成氢键.
(3)COCl2 俗称光气,分子中C原子采取sp2杂化成键;其中分子中的共价键含有C(填序号):
A 2个σ键 1个π键 B 2个键π C 3个σ键、1个π键
Ⅱ:海水中富含氯元素.
(4)KCl广泛应用于医药和农业,KCl晶体中基态的Cl-电子排布式为1s22s22p63s23p6
(5)下列是IA族的Li、Na、K三种金属元素的电离能
| X | Y | Z | |
| 第一电离能(KJ/mol) | 526.2 | 502.8 | 425.2 |
(6)RCl用作有机机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图乙所示.R的元素符号是Cu,每个Cl-周围最近的Cl-12个.已知该晶体密度为1.15 g/cm3,则晶胞中最近的R+和Cl-之间的距离为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{4×99.5}{1.15×6.02×1{0}^{23}}}$cm(NA=6.02×1023/mol,只写出计算表达式即可)
7.下列物质中,不能电离出酸根离子的是( )
| A. | Na2CO3 | B. | KNO3 | C. | KOH | D. | H2SO4 |
14.下列物质中,pH最小的是( )
| A. | 食盐水 | B. | 纯净水 | C. | 食醋 | D. | 石灰水 |
4.下列实验过程正确的是( )
| A. | 用酒精萃取碘水中的碘 | |
| B. | 海盐经过溶解、过滤、蒸发制纯净的NaCl | |
| C. | CO2气体混有少量HCl气体,将气体通过盛有饱和Na2CO3中溶液的洗气瓶以除去HCl气体 | |
| D. | 分液操作时,分液漏斗中先把下层液体从下口放出,再把上层液体从上口倒出 |
11.有500ml 含Na2CO3与Na2SO4的混合溶液,向其中加入足量的BaCl2溶液,得到66.3g白色沉淀,向所得沉淀中加入足量HCl,最后剩余46.6g沉淀,则溶液中Na+的物质的量浓度为( )
| A. | 0.6mol/L | B. | 1mol/L | C. | 1.2mol/L | D. | 0.5mol/L |
8. 下列实验操作正确的是( )
下列实验操作正确的是( )
 下列实验操作正确的是( )
下列实验操作正确的是( )| A. | 可用磨口玻璃瓶保存NaOH溶液 | |
| B. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| C. | 用装置甲分液,放出水相后再从分液漏斗下口放出有机相 | |
| D. | 用装置乙加热分解NaHCO3固体 |
9.25℃时,某溶液中由水电离产生的c(H+)和c(OH-)的乘积为1×10-18,下列说法中正确的是( )
| A. | 该溶液的pH一定是9 | B. | 该溶液的溶质可能是可水解的盐 | ||
| C. | 该溶液的溶质可能是酸或碱 | D. | 不可能有这样的溶液 |