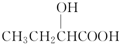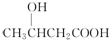题目内容
19.下列叙述正确的是( )| A. | 1.7克-OH中含有的电子数为NA | |
| B. | 42g乙烯与丙烯的混合气体中含碳原子数为3NA | |
| C. | 二氯乙烯的结构简式:CH2=C(Cl)2 | |
| D. | 乙烯和乙醇的混合物共0.1mol,完全燃烧所消耗的氧气的分子数一定为0.6 NA |
分析 A、求出-OH的物质的量,然后根据-OH中含9个电子来分析;
B、乙烯和丙烯的最简式均为CH2;
C.二氯乙烯存在同分异构体,可能是1,1-二氯乙烯或1,2-二氯乙烯;
D、1mol乙烯和乙醇均消耗3mol氧气.
解答 解:A、1.7g-OH的物质的量为0.1mol,而-OH中含9个电子,故0.1mol-OH中含0.9mol电子即0.9NA个,故A错误;
B、乙烯和丙烯的最简式均为CH2,故42g混合物中含有的CH2的物质的量为n=$\frac{42g}{14g/mol}$=3mol,故含3NA个碳原子,故B正确;
C.有两种可能,1,2-二氯乙烯,结构简式为CHCl=CHCl,1,1-二氯乙烯,结构简式为CH2=C(Cl)2,故C错误;
D、1mol乙烯和乙醇均消耗3mol氧气,故0.1mol乙烯和乙醇的混合物消耗0.3mol氧气即0.3NA个氧气分子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是微粒结构、微粒数的计算、物质结构等知识,注意有机物的同分异构体的分析,题目难度中等,

练习册系列答案
相关题目
19.下列各组离子在溶液中能大量共存的是( )
| A. | Ba2+、Cu2+、NO3-、SO42- | B. | K+、Na+、SO42-、Cl- | ||
| C. | CO32-、H+、Na+、K+ | D. | H+、Cl-、NO3-、Ag+ |
7.下列有关分离和提纯的说法正确的是( )
| A. | 除去NaCl溶液中少量CaCl2:加入适量K2CO3 | |
| B. | 用蒸馏的方法从海水中得到淡水 | |
| C. | 用酒精可以从碘水中萃取碘 | |
| D. | 用浓硫酸除去氨气中混有的水蒸气 |
14.下列关于常见有机物的说法正确的是( )
| A. | 乙烯和甲苯都能与溴水、H2反应 | |
| B. | 聚乙烯的结构简式为CH2=CH2 | |
| C. | 甲苯既能使溴的水溶液褪色,又能在光照下与溴蒸气发生取代反应 | |
| D. | 可用酸性高锰酸钾溶液鉴别乙烯和甲烷或除去甲烷中的乙烯 |
4.2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
| A. | 分子中碳原子不在一条直线上 | B. | 比丁烷更易液化 | ||
| C. | 1mol丙烷完全燃烧需消耗氧气5mol | D. | 光照下能够发生取代反应 |
11.对于化学反应方向的确定不仅与焓变(△H)有关,也与温度(T)、熵变(△S)有关,实验证明,化学反应的方向应由△H-T△S确定,若△H-T△S<0,则自发进行,否则不能自发进行.下列说法中,正确的是( )
| A. | 在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 | |
| B. | 温度、压强一定时,熵增加的反应一定能自发进行 | |
| C. | 反应焓变是决定反应能否自发进行的唯一因素 | |
| D. | 固体的溶解过程只与焓变有关 |