题目内容
18.下列反应的离子方程式书写正确的是( )| A. | 锌溶于醋酸:Zn+2H+=Zn2++H2↑ | |
| B. | 氯气与溴化钠溶液:2Br-+Cl2=Br2+2Cl- | |
| C. | 氯化铝与氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 氯气溶于水:Cl2+H2O?2H++Cl-+ClO- |
分析 A.醋酸为弱酸,应保留化学式;
B.二者反应生成氯化钠和溴单质;
C.氨水为弱电解质,应保留化学式;
D.次氯酸为弱酸应保留化学式.
解答 解:A.锌溶于醋酸,离子方程式:Zn+2CH3COOH=Zn2++H2↑+2CH3COO-,故A错误;
B.氯气与溴化钠溶液,离子方程式:2Br-+Cl2=Br2+2Cl-,故B正确;
C.氯化铝与氨水,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.氯气溶于水,离子方程式:Cl2+H2O?H++Cl-+HClO,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子方程式中,弱电解质应保留化学式.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
9.下列离子方程式中,正确的是( )
| A. | 向NaOH溶液中加入少量Mg(HCO3)2溶液:2OH-+Mg2+═Mg(OH)2↓ | |
| B. | 向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:2HCO3-+Ba2++2H++SO42-═BaSO4↓+2H2O+2CO2↑ | |
| C. | 酸性KMnO4溶液与H2O2反应:2MnO4-+10H++3H2O2═2Mn2++3O2↑+8H2O | |
| D. | 向Fe(NO3)3溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 |
13.下列化学用语表示正确的是( )
| A. | 氯气的电子式:Cl:Cl | |
| B. | 乙烯的结构简式CH2CH2 | |
| C. | 钠原子的结构示意图: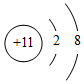 | |
| D. | 硫酸亚铁的电离方程式FeSO4═Fe2++SO42- |
10.某溶液可能存在Na+、Ba2+、Mg2+、Fe3+、Br-、CO32-、Cl-等离子,某学生进行下列实验:取少量原溶液,测得溶液呈强碱性,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色.关于该原溶液的推测正确的是( )
| A. | 溶液中可能存在Mg2+和Fe3+ | B. | 溶液中可能存在Br-和Cl- | ||
| C. | 溶液可能存在Ba2+和Cl- | D. | 溶液中一定存在Na+和CO32- |
8.普伐他汀是一种调节血脂的药物,其结构如图所示.下列关于普伐他汀的性质描述不正确的是( )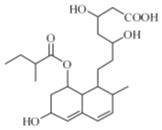

| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可消耗4molNaOH、2molBr2 |
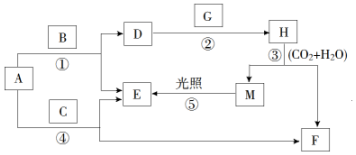
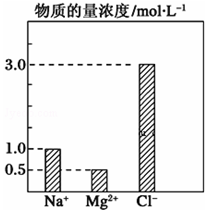 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题: