题目内容
3.在一定温度不同压强下,可逆反应2X(g)?2Y(g)+Z(g),生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系如图所示,正确的是(已知p1<p2)( )| A. | 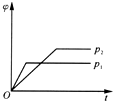 | B. | 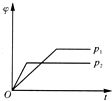 | C. | 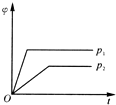 | D. | 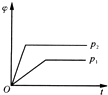 |
分析 该反应前后气体体积增大,增大压强,反应速率都增大,则反应达到平衡状态的时间缩短,增大压强平衡逆向移动,生成物含量较低,据此分析解答.
解答 解:增大压强,反应速率增大,到达平衡所用时间短,所以p1<p2;
相对于p1来说,p2就是增大压强.该可逆反应是一个正向气体分子数增加的反应,所以增大压强,平衡应向减少Z的方向移动,Z在混合气体中的体积分数就要减小,所以B图象正确,故选B.
点评 本题考查图象分析,为高频考点,侧重考查学生分析判断能力,明确压强对化学反应速率、化学平衡移动影响原理是解本题关键,会根据图象中“先拐先平数值大”确定压强大小,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在常温常压下,1mol氦气含有的原子数为NA | |
| B. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| C. | 常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 | |
| D. | 物质的量浓度为1 mol•L-1的K2SO4溶液中,含2NA个K+ |
15.①中和法 ②氧化还原法 ③沉淀法.其中可用于处理污水的是( )
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
13.常温下,某酸HA的电离常数:K=1×10-5,下列说法正确的是( )
| A. | HA溶液中加入NaA固体后,$\frac{c(HA)c(O{H}^{-})}{c({A}^{-})}$减小 | |
| B. | 常温下,0.1mol/LHA溶液中水电离的c(H+)为10-13mol/L | |
| C. | 常温下,0.1mol/LNaA溶液水解常数为10-9 | |
| D. | NaA溶液中加入HCl溶液至恰好完全反应,存在关系:2c(Na+)═c(A-)+c(Cl-) |
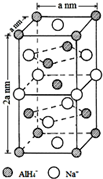 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.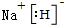 .
.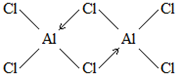 (标明配位键).
(标明配位键).