题目内容
19.常温下,某氨水的pH=x,某盐酸的pH=Y,已知x+y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是( )| A. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B. | c(Cl-)>c( NH4+)>c(OH-)>c(H+) | ||
| C. | c( NH4+)>c(Cl-)>c(OH-)>c(H+) | D. | c( NH4+)+c(NH3.H2O)=c(Cl-) |
分析 常温下,某氨水的pH=x,某盐酸的pH=y,已知x+y=14,则盐酸中c(H+)=10-ymol/L,氨水中c(OH-)=10 x-14mol/L=10-ymol/L,HCl是强电解质、一水合氨是弱电解质,所以氨水浓度大于稀盐酸,二者等体积混合,混合溶液中的溶质为氯化铵和一水合氨,一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,结合电荷守恒判断.
解答 解:常温下,某氨水的pH=x,某盐酸的pH=y,已知x+y=14,则盐酸中c(H+)=10-ymol/L,氨水中c(OH-)=10 x-14mol/L=10-ymol/L,HCl是强电解质、一水合氨是弱电解质,所以氨水浓度大于稀盐酸,二者等体积混合,混合溶液中的溶质为氯化铵和一水合氨,一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,
A.一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,所以c(OH-)>c(H+),故A错误;
B.一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,所以c(OH-)>c(H+),根据电荷守恒得c( NH4+)>c(Cl-),一水合氨电离程度较小,所以溶液中离子浓度大小顺序是c( NH4+)>c(Cl-)>c(OH-)>c(H+),故B错误;
C.根据B知,溶液中离子浓度大小顺序是c( NH4+)>c(Cl-)>c(OH-)>c(H+),故C正确;
D.氨水浓度大于稀盐酸,所以c( NH4+)+c(NH3.H2O)>c(Cl-),故D错误;
故选C.
点评 本题考查酸碱混合溶液定性判断及离子浓度大小比较,正确判断氨水和稀盐酸浓度相对大小是解本题关键,结合电解质溶液酸碱性及电荷守恒分析解答,题目难度不大.

练习册系列答案
相关题目
9.把10.6g碳酸钠溶于水制成100ml溶液,再从中取出10ml溶液,下列说法正确的是( )
| A. | 碳酸钠的物质的量浓度为0.1mol/L | B. | 碳酸钠的物质的量为0.1mol | ||
| C. | c(Na+)=0.2mol/L | D. | c(Na+)=2mol/L |
10.若7x%和x%的两种液体等体积混合,其质量分数大于4x%,此溶质可能是( )
| A. | H2SO4 | B. | NH3•H2O | C. | NaOH | D. | 乙醇 |
7.下面有关电化学的图示,完全正确的是( )
| A. | 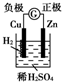 Cu-Zn原电池 | B. | 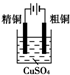 粗铜的精炼 | ||
| C. | 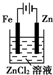 铁片镀锌 | D. | 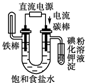 验证NnCl溶液(含酚酞) |
14.某温度下,浓度都是1mol•L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为:[X2]=0.4mol•L-1,[Y2]=0.8mol•L-1,[Z]=0.4mol•L-1,则该反应的反应式可表示为( )
| A. | X2+2Y2?2XY2 | B. | 2X2+Y2?X2Y | C. | 3X2+Y2?2X3Y | D. | X2+3Y2?2XY3 |
4.下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合,c(Cl-)>c(NH${\;}_{4}^{+}$)>c(OH-)>c(H+) | |
| B. | 10mL0.1mol/L NH4Cl溶液与5mL0.2mol/LNaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) | |
| C. | 10mL0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 10mL0.5mol/LCH3COONa溶液与6mL 1mol/L盐酸混合,c(Na+)=c(Cl-)>c(H+)>c(OH-) |
11.下列物质中含原子数最多的是( )
| A. | 6.4g O2 | B. | 8.8g CO2 | C. | 0.1mol N2 | D. | 3.01×1022个H2O |
8.下列关于浓硝酸和浓硫酸的叙述正确的是( )
| A. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| B. | 浓硝酸具有不稳定性,实验室里应保存在棕色瓶中 | |
| C. | 常温下,浓硝酸可以跟铜缓慢反应,浓硫酸可与铜片迅速反应 | |
| D. | 实验室可以用浓硝酸来制氢气 |
9.氢能是未来能源结构中最具发展潜力的清洁能源之一.目前已有专家已研究出用淀粉或纤维素与水在酶作用下转变为二氧化碳和氢气的方法制氢气.下列说法错误的是( )
| A. | 从整个循环来看,利用该方法得到的氢能来源于太阳能 | |
| B. | 上述制氢气的化学方程式可表示为:(C6H10O5)n+7nH2O$\stackrel{酶}{→}$ 6nCO2↑+12nH2↑ | |
| C. | 氢元素的三种同素异形体${\;}_{1}^{1}H$、${\;}_{1}^{2}H$、${\;}_{1}^{3}H$,能形成六种单质 | |
| D. | 从化学的本质看该反应属于氧化还原反应 |