题目内容
三氟化氮(NF3)在微电子工业中有重要用途,它在潮湿的空气中与水蒸气反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.NF3分子中含有非极性共价键 |
| B.NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
C
解析试题分析:A、三氟化氮中只含有氮氟键,属极性共价键,错误;B、NF3与水反应的产物中NO,遇空气会变为红棕色,错误;C、可以的,因为产物均能溶于石灰水,正确;D、反应过程中,被氧化与被还原的元素的物质的量之比为1:2,错误。
考点:考查有关化学键,氧化还原反应的概念以及元素及其化合物的知识。

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
硫的卤化物(S2X2)是广泛用于橡胶工业的硫化剂,S2C12分子结构如图所示。遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )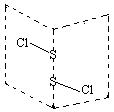
| A.稳定性S2C12>S2Br2 |
| B.反应中,生成1molSO2,转移电子为3mol |
| C.分子中同时含有极性键和非极性键且各原子都满足8电子稳定结构 |
| D.因为S-Cl键能比S-Br键能大,S2C12沸点比S2Br2高 |
下列说法正确的是( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
| A.①③⑤ | B.②④⑤ | C.②③④ | D.①③ |
能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是
| A.浓氨水 | B.NaOH溶液 | C.CCl4 | D.AgNO3溶液 |
下列有关化学键与晶体结构的说法正确的是
| A.两种元素组成的分子中一定只有极性键 |
| B.离子化合物的熔点一定比共价化合物的高 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阴离子的化合物一定含有阳离子 |
物质的变化需要改变微粒之间的相互作用,所克服的作用属于同种类型的是
| A.Br2(l)和I2(s)分别受热气化 | B.NaBr和HI分别在水中电离 |
| C.硅和铁分别受热熔化 | D.氯化氢和蔗糖分别溶解于水 |
科学家曾预言一种可用作炸药的物质,分子式为C(N3)4,其爆炸反应方程式为:C(N3)4=C+6N2↑,下列说法一定正确的是
| A.该物质为离子晶体 |
| B.该物质可通过C60吸附N2直接制得 |
| C.18g该物质完全分解产生13.44LN2 |
| D.C(N3)4中碳元素为正价 |
关于含正离子N5+的化合物N5ASF6,下列叙述中错误的是( )
| A.N5+共有34个核外电子 |
| B.N5+中氮原子间以离子键结合 |
| C.化合物N5ASF6中AS的化合价为+1价 |
| D.化合物N5ASF6为离子化合物 |