题目内容
下列说法正确的是( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
| A.①③⑤ | B.②④⑤ | C.②③④ | D.①③ |
D
解析试题分析:①、如过氧化钠中含有离子键和非极性键,氢氧化钠中含有离子键和极性键,正确;②、同位素的化学性质相似,但物理性质不同,错误;③、活泼金属与活泼非金属组成的混合物是离子化合物,不活泼金属和活泼不活泼非金属可能形成共价化合物,正确;④、铵盐是离子化合物,所以由非金属元素组成的化合物不一定是共价化合物,正确;⑤、稀有气体为单原子分子,原子本身为稳定结构,不含共价键,错误,故D项正确。
考点:本题考查化学键与化合物的有关判断。

 高中必刷题系列答案
高中必刷题系列答案近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150℃,燃烧热极高。下列说法肯定错误的是
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D.氢铝化合物中可能存在组成为的物质(n为正整数) |
下列变化需克服相同类型作用力的是
| A.碘和干冰的升华 | B.硅和C60的熔化 | C.氯化氢和氯化钾的溶解 | D.溴和汞的气化 |
有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
| A.N2O与SiO2为等电子体、具有相似的结构(包括电子式) |
B.N2O的电子式可表示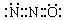 |
| C.N2O与CO2均不含非极性键 |
| D.N2O为三角形分子 |
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N—N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )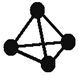
| A.N4属于一种新型的化合物 | B.N4晶体熔点高,硬度大 |
| C.相同质量的N4能量高于N2 | D.1mol N4转变成N2将吸收882 kJ热量 |
下列有关σ键和π键的说法正确的是
| A.σ键是镜像对称,而π键是轴对称 |
| B.π键是由两个p电子“头碰头”重叠形成的 |
| C.σ键可沿键轴自由旋转而不影响键的强度 |
| D.π键比σ键重叠程度大,形成的共价键强 |
已知:N2+O2 2NO △H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为
2NO △H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为
| A.812 kJ/mol | B.632 kJ/mol | C.1264 kJ/mol | D.1624 kJ/mol |
三氟化氮(NF3)在微电子工业中有重要用途,它在潮湿的空气中与水蒸气反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.NF3分子中含有非极性共价键 |
| B.NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
下列说法正确的是
| A.含有离子键的化合物一定是离子化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.所有物质都含有共价键 |
| D.均由非金属元素形成的化合物不可能是离子化合物 |