题目内容
硫的卤化物(S2X2)是广泛用于橡胶工业的硫化剂,S2C12分子结构如图所示。遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )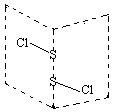
| A.稳定性S2C12>S2Br2 |
| B.反应中,生成1molSO2,转移电子为3mol |
| C.分子中同时含有极性键和非极性键且各原子都满足8电子稳定结构 |
| D.因为S-Cl键能比S-Br键能大,S2C12沸点比S2Br2高 |
D
解析试题分析:A. S2C12和S2Br2结构相似。元素的非金属性越强,其对应的化合物就越稳定。所以稳定性S2C12>S2Br2。正确。B. 在2S2C12+2H2O=SO2↑+3S↓+4HCl反应中,S的化合价由反应前S2C12的+1变为反应后SO2中的+4价和S的0价。所以生成1molSO2,转移电子为3mol。正确。C.在分子中S-Cl键是极性共价键; S-S键是非极性共价键.每个原子都都满足8电子稳定结构。正确。D.二者都是分子晶体,通过分子间作用力结合。分子间作用力越大,克服分子间作用力使物质融化或汽化消耗的能量就越高,熔沸点就越高。故S2C12沸点比S2Br2高是因为S2C12的分子间作用力比S2Br2的大。错误。
考点:考查有关广泛用于橡胶工业的硫化剂S2C12的结构、性质等的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150℃,燃烧热极高。下列说法肯定错误的是
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D.氢铝化合物中可能存在组成为的物质(n为正整数) |
下列物质中,既含有离子键又含有非极性键的是
| A.Na2O2 | B.CO2 | C.苯 | D.NH4Cl |
下列物质中,含有非极性共价键的是
| A.H2 | B.H2O | C.NaCl | D.NaOH |
医学上在对抗癌物质的研究中发现 具有抗癌作用,而
具有抗癌作用,而 没抗癌作用。对此下列叙述正确的是( )
没抗癌作用。对此下列叙述正确的是( )
| A.两者互为同分异构体,都是以Pt原子为中心的四面体结构 |
| B.两者互为同分异构体,都是以Pt原子为中心的平面结构 |
| C.两者为同一物质,都是以Pt原子为中心的四面体结构 |
| D.两者为同一物质,都是以Pt原子为中心的平面结构 |
下列变化需克服相同类型作用力的是
| A.碘和干冰的升华 | B.硅和C60的熔化 | C.氯化氢和氯化钾的溶解 | D.溴和汞的气化 |
有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
| A.N2O与SiO2为等电子体、具有相似的结构(包括电子式) |
B.N2O的电子式可表示 |
| C.N2O与CO2均不含非极性键 |
| D.N2O为三角形分子 |
三氟化氮(NF3)在微电子工业中有重要用途,它在潮湿的空气中与水蒸气反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.NF3分子中含有非极性共价键 |
| B.NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法不正确的是( )
| A.1 mol NH5中含有5 NA个N—H键(NA表示阿伏加德罗常数) |
| B.NH5中既有共价键又有离子键 |
C.NH5的电子式为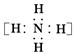 + +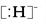 |
D.它与水反应的离子方程式为NH4++H-+H2O NH3·H2O+H2↑ NH3·H2O+H2↑ |