题目内容
18.下列离子方程式正确的是( )| A. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 | |
| B. | NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O | |
| C. | NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- | |
| D. | FeCl3溶液腐蚀印刷电路:Fe3++Cu=Fe2++Cu2+? |
分析 A.碘离子过量,硝酸根离子、三价铁离子都被还原;
B.高锰酸根离子酸性环境下氧化亚硝酸根离子生成硝酸根离子;
C.氢氧化钡过量反应生成碳酸钡、碳酸氢钠和水;
D.电荷不守恒.
解答 解:A.硝酸铁溶液中滴加足量HI溶液,铁离子和硝酸根离子都参与反应,离子方程式为:Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO↑+6H2O,故A错误;
B.NaNO2溶液中加入酸性KMnO4溶液,离子方程式:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O,故B正确;
C.NaHCO3溶液中加入过量的Ba(OH)2溶液,离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O,故C错误;
D.FeCl3溶液腐蚀印刷电路,离子方程式:2Fe3++Cu=2Fe2++Cu2+?,故D错误;
故选:B.
点评 本题考查了离子方程式的书写判断,题目难度中等,学生灵活应用基础知识的能力,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循客观事实、原子个数、电荷数守恒规律.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
8. 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
则A原子的价电子排布式为3s2.
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
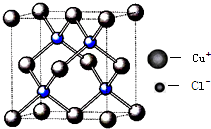
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
9.对二甲苯 ( PX )是生产矿泉水瓶 (聚对苯二甲酸乙二酯,简称 PET )的必要原料,生产涉及的反应之一如下:
5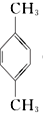 (PX)+12MnO4-+36H+→5
(PX)+12MnO4-+36H+→5 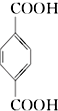 (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )
5
 (PX)+12MnO4-+36H+→5
(PX)+12MnO4-+36H+→5  (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )| A. | PTA 是该反应的氧化产物 | |
| B. | PTA 与乙二醇通过缩聚反应即可生产 PET 塑料 | |
| C. | PX 分子含有苯环的同分异构体还有 3 种 | |
| D. | 该反应消耗 1molPX,共转移 10mol电子 |
6.下列叙述正确的是( )
| A. | 乙醛和甲酸两者都能发生银镜反应,所以它们互为同系物 | |
| B. | 营养物质中的多糖、油脂、蛋白质在一定条件下都可以发生水解 | |
| C. | 氨基酸和氯乙烯都能通过加聚反应生成高分子化合物 | |
| D. | 通过对煤的分馏,可以提高煤的利用率 |
10.下列说法不正确的是( )
| A. | 构成有机物的骨干元素是碳 | |
| B. | 构成地壳的骨干元素是Si,在二氧化硅晶体中每个Si原子周围结合4个O原子,每个O原子周围结台2个Si原子,[SiO4]四面体向空间无限伸展,形成立体网状结构 | |
| C. | 单质Si是制作计算机芯片的主要材料,SiO2是制取光导纤维的主要材料 | |
| D. | 空气中含量最大的元素是N.海水中含量最大的元索是C1,太阳系中含量最大的元素是H |
8.如图所示装置在常温下工作(溶液体积变化忽略不计),闭合K,灯泡发光,下列叙述中不正确的是( )
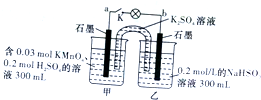

| A. | 电池工作时,甲烧杯中由烧杯中由水电离出的c(H+)逐渐减小 | |
| B. | 电池工作时,盐桥中的“K+”移向甲烧杯,外电路的方向是从b到a | |
| C. | 当电路中有1.204×1021个电子转移时,乙烧杯中溶液的pH约为2 | |
| D. | 乙池中的氧化产物为SO${\;}_{4}^{2-}$ |
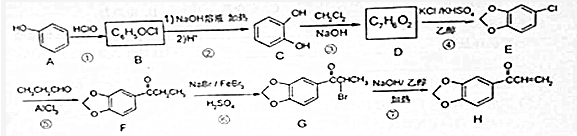
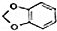 .
.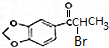 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaBr+H2O.
+NaBr+H2O. 等(写出其中一种的结构简式).
等(写出其中一种的结构简式). 的合成路线.
的合成路线. CH3COOCH2CH3+H2O;苯制取环己烷:
CH3COOCH2CH3+H2O;苯制取环己烷: .
.