题目内容
16.下列叙述中,正确的是( )| A. | 钢铁腐蚀的负极反应为:Fe-3e-=Fe3+ | |
| B. | 碱性介质甲烷燃料电池的正极反应为:O2+2H2O+4e-═4OH- | |
| C. | Mg-Al及NaOH溶液构成的原电池中负极材料为Mg | |
| D. | 氯碱工业中阳极上产生的气体比阴极上产生的气体多 |
分析 A、钢铁吸氧腐蚀负极铁失电子生成亚铁离子;
B、碱性介质甲烷燃料电池的正极为氧气得电子发生还原反应;
C、Mg-Al及NaOH溶液构成的原电池,铝作负极;
D、氯碱工业中阳极上产生氯气,阴极上产生氢气.
解答 解:A、钢铁吸氧腐蚀的负极反应为,Fe-3e-═Fe2+,故A错误;
B、碱性介质甲烷燃料电池的正极为氧气得电子发生还原反应,反应为:O2+2H2O+4e-═4OH-,故B正确;
C、Mg-Al及NaOH溶液构成的原电池,铝与氢氧化钠反应而镁不反应,则铝作负极,故C错误;
D、氯碱工业中阳极上产生氯气,阴极上产生氢气,则产生的气体一样多,故D错误;
故选:B.
点评 本题考查了电化学的原理分析应用,掌握原电池和电解池原理是解题关键,题目较简单.

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
6.分类法是一种行之有效、简单易行的科学方法.某同学用如下形式对所学知识进行分类,甲与乙、丙、丁是包含关系.其中正确的是( )
| A. | 甲(电解质):乙、丙、丁(一水合氨、水、盐酸) | |
| B. | 甲(腐蚀品):乙、丙、丁(浓硫酸、烧碱、硝酸) | |
| C. | 甲(有机化合物):乙、丙、丁(甲烷、醋酸钠、乙醛) | |
| D. | 甲(合成高分子材料):乙、丙、丁(光导纤维、涤纶、玻璃) |
7.下列有关实验操作或判断不正确的是( )
| A. | 配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 | |
| B. | 用干燥的pH试纸测定氯水的pH | |
| C. | 配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 | |
| D. | 在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 | |
| E. | 观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,观察. | |
| F. | 制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中 |
4.用试剂制备下列气体和性质实验中,由现象得出的结论错误的是( )
| 选项 | 试剂 | 试纸或试液或气体 | 现象 | 结论 |
| A | 浓氨水、生石灰 | 湿润的红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
| B | 亚硫酸钠、浓硫酸 | 澄清石灰水溶液 | 溶液先变浑浊后又澄清 | 溶解度CaSO3大于Ca(HSO3)2 |
| C | 浓盐酸、MnO2加热 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
| D | 稀硝酸、铜 | 产生无色气体通入空气 | 气体变为红棕色 | 无色气体为NO |
| A. | A | B. | B | C. | C | D. | D |
8.氢气、甲烷、乙醇均可设计成燃料电池.下列有关燃料电池的说法错误的是( )
| A. | 氢气、甲烷、乙醇在燃料电池中作负极材料 | |
| B. | 氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物可回收利用 | |
| C. | 碱性介质下的乙醇燃料电池负极反应为:C2H5OH-12e-═2CO2↑+3H2O | |
| D. | 碱性介质下甲烷燃料电池的正极反应为:O2+2H2O+4e-═4OH |
5.下列反应为氧化还原反应,且氧化剂和还原剂为同种物质的是( )
| A. | SO2+Cl2+2H2O=H2SO4+2HCl | B. | 3CO2+4NaOH=2NaHCO3+Na2CO3+H2O | ||
| C. | Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO | D. | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
1.下列溶液中c(Cl-)与50mL 1mol•L-1AlCl3溶液中c(Cl-)相等的是( )
| A. | 75 mL 1.5 mol•L-1的MgCl2溶液 | B. | 75 mL 4 mol•L-1的NH4Cl溶液 | ||
| C. | 150 mL 2 mol•L-1的KCl溶液 | D. | 150 mL 1 mol•L-1的NaCl溶液 |
 2,3-二甲基戊烷
2,3-二甲基戊烷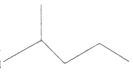 表示的分子式C6H14;
表示的分子式C6H14;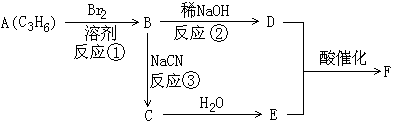
 .
.