题目内容
下列实验操作要用到玻璃棒的是( )
①溶解 ②过滤 ③蒸发 ④向容量瓶转移液体 ⑤蒸馏 ⑥分液.
①溶解 ②过滤 ③蒸发 ④向容量瓶转移液体 ⑤蒸馏 ⑥分液.
| A、全部 | B、②③④⑤ |
| C、①②③④ | D、①③④⑤⑥ |
考点:过滤、分离与注入溶液的仪器,蒸发、蒸馏与结晶的仪器
专题:化学实验常用仪器
分析:根据玻璃棒的作用来考虑:溶解固体时搅拌是加速溶解的,过滤时是引流作用,测溶液酸碱性或测PH值用玻璃棒蘸取待测液,蒸发时搅拌防止局部温度过高使液滴飞溅,配制一定体积的物质的量浓度的溶液用玻璃棒引流.
解答:
解:①溶解固体时搅拌是加速溶解的,故①正确;
②过滤时用玻璃棒引流,故②正确;
③蒸发时搅拌防止局部温度过高使液滴飞溅,故③正确;
④转移液体时用玻璃棒引流,故④正确;
⑤蒸馏用蒸馏烧瓶,不用玻璃棒,故⑤错误;
⑥分液用分液漏斗,不用玻璃棒,故⑥错误;
故选C.
②过滤时用玻璃棒引流,故②正确;
③蒸发时搅拌防止局部温度过高使液滴飞溅,故③正确;
④转移液体时用玻璃棒引流,故④正确;
⑤蒸馏用蒸馏烧瓶,不用玻璃棒,故⑤错误;
⑥分液用分液漏斗,不用玻璃棒,故⑥错误;
故选C.
点评:本题考查了玻璃棒在各个实验中的作用,题目难度不大,明确实验操作及操作的目的即可解答,注重对操作的理解来解答.

练习册系列答案
相关题目
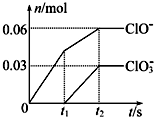 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、反应中转移电子的物质的量是0.21 mol |
| B、ClO3-的生成是由于温度升高引起的 |
| C、苛性钾溶液中KOH的质量为5.04g |
| D、反应中氧化剂和还原剂的物质的量之比为7:3 |
根据表中提供的数据判断下列说法不正确的是( )
| 化学式 | 电离常数(25℃) |
| HCN | K=5.0×10-10 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
| A、等浓度等体积的NaCN、NaHCO3溶液混合:c(Na+)+c(H+)=c(HCO3-)+c(CN-)+c(OH-)+2c(CO32-) | ||
B、若NaCN的水解平衡常数为:Kh=
| ||
| C、等浓度等体积的NaCN和NaCl溶液中离子数目前者大于后者 | ||
| D、过量CO2通入NaCN溶液中:CO2+H2O+CN-=HCO3-+HCN |
下列物质性质与应用对应关系正确的是( )
| A、过氧化钠可以与CO2反应放出O2,可用于潜艇中的供氧剂 |
| B、硅酸钠溶液呈碱性,可涂在木材的表面作耐火剂 |
| C、SO2具有氧化性,可用于纸浆的漂白 |
| D、明矾溶于水可形成有氢氧化铝胶体,可用于自来水的杀菌消毒 |
下列叙述正确的是( )
| A、向海水中加碱、过滤、加酸,之后浓缩结晶、过滤、干燥、电解能得到金属镁 |
| B、将淡黄色的过氧化钠粉末加入到石蕊试液中,石蕊试液先变红后褪色 |
| C、合金性能一般优于纯金属,钢铁比纯铁具有更好的抗锈蚀能力 |
| D、将碘水倒入分液漏斗,加适量乙醇振荡后静置,可将碘萃取到乙醇中 |
已知室温时,0.1mol?L-1某一元酸HA的电离平衡常数约为1×10-7,下列叙述错误的是( )
| A、该溶液的pH=4 |
| B、此溶液中,HA约有0.1%发生电离 |
| C、加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |

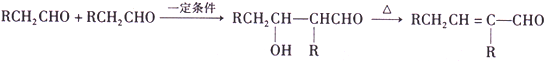
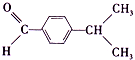 )合成兔耳草醛的路线如下:
)合成兔耳草醛的路线如下: