题目内容
3.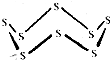 黑火药是我国古代的四大发明之一,KNO3、C及S8 (结构式如图所示)爆炸生成K2S、CO2和N2,下列说法正确的是( )
黑火药是我国古代的四大发明之一,KNO3、C及S8 (结构式如图所示)爆炸生成K2S、CO2和N2,下列说法正确的是( )| A. | 该反应属于置换反应 | |
| B. | 该反应中氧化剂只有KNO3 | |
| C. | 32g S8含有S-S的数目约为6.02×1023 | |
| D. | 还原产物为CO2 |
分析 反应S8+16KNO3+24C═8K2S+8N2↑+24CO2↑中,N和S元素化合价降低,被还原,C元素化合价升高,被氧化,据此分析.
解答 解:A.反应体系中反应物是三种,生成物也是三种,所以不是置换反应,故A错误;
B.反应中N和S元素化合价降低,被还原,C元素化合价升高,所以还原剂是C、氧化剂是S8和KNO3,故B错误;
C.消耗32gS8即$\frac{1}{8}$mol,而1mol中S8中含有8mol的S-S,所以32g S8含有S-S的数目约为6.02×1023,故C正确;
D.C元素化合价升高,所以还原剂是C被氧化,所以二氧化碳是氧化产物,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题注意把握元素化合价的变化,从化合价的角度理解氧化还原反应.

练习册系列答案
相关题目
13.对下列实验现象的解释正确的是( )
| 现象 | 解释 | |
| A | KI淀粉溶液通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| B | 向溴水中通入SO2,溶液变无色 | SO2表现还原性 |
| C | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
| D | 铜片放入浓硫酸中,无明显变化 | 说明铜在冷的浓硫酸中发生钝化 |
| A. | A | B. | B | C. | C | D. | D |
14.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 相同质量的铝,分别与足量的盐酸和氢氧化钠溶液反应放出的氢气体积一定不相同 | |
| B. | 56gFe与足量盐酸反应转移电子数为3NA | |
| C. | 任何条件下,22.4LNH3与18gH2O所含电子数均为10NA | |
| D. | 46gNO2和N2O4的混合物含有的原子数为3NA |
11.四种仪器中,不能用来加热的是( )
| A. |  烧杯 | B. |  容量瓶 | C. |  试管 | D. |  烧瓶 |
18.下列有关叙述正确的是( )
| A. | 在NaHS溶液中滴人少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大,pH增大 | |
| B. | 常温下,由于HCO3-水解显碱性,所以饱和NaHCO3溶液显碱性 | |
| C. | 泡沫灭火器是利用Al2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 | |
| D. | 配制氯化铝溶液时,先将氯化铝溶于浓硫酸,再加水稀释 |
8.化学在生活中应用广泛,下列物质性质与对应用途错误的是( )
| A. | 明矾易水解生成胶体,可用作净水剂 | |
| B. | 晶体硅熔点高硬度大,可用作芯片 | |
| C. | 氮气化学性质稳定,可用作粮食保护气 | |
| D. | 溴化银见光易分解,可用作胶片感光剂 |
2.下列说法不正确的是( )
| A. | 铜呈紫红色.可与氯化铁溶液反应制作印刷电路板 | |
| B. | 可用丁达尔效应区分胶体和溶液 | |
| C. | 工业上用焦炭在高温下还原二氧化硅可直接得到高纯度的硅 | |
| D. | 镁合金大量用于制造火箭、导弹和飞机的部件 |
19.由短周期元素组成的中学常见物质A、B、C、D、E、X,存在如图转化关系:A$\stackrel{E}{→}$B$\stackrel{E}{→}$C$\stackrel{X}{→}$D(部分生成物和反应条件略去).下列推断错误的是( )
| A. | 若D与盐酸反应,可生成A和B,则X一定是H2O | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| D. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B |
20.下列电离方程式中正确的是( )
| A. | HNO3═H++N5++3O2- | B. | Ca(OH)2═Ca2++(OH-)2 | ||
| C. | AlCl3═Al+3+3Cl- | D. | Al2(SO4)3═2Al3++3SO42- |