题目内容
16.二氧化硫不具有的性质是( )| A. | 会形成酸雨 | B. | 漂白性 | C. | 还原性 | D. | 无色无味 |
分析 二氧化硫为酸性氧化物,可与水、碱以及碱性氧化物反应,S元素化合价为+4价,处于中间价态,既具有氧化性也具有还原性,另外还具有漂白性,以此解答.
解答 解:二氧化硫为无色、具有刺激性气味的气体,可与水、碱以及碱性氧化物反应,具有漂白性、氧化性和还原性,可形成酸雨,只有D错误.
故选D.
点评 本题考查二氧化硫的性质,为高频考点,侧重于双基的考查,有利于培养学生良好的科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
7. 食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益,其分子结构如图所示.下列说法不正确的是 ( )
食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益,其分子结构如图所示.下列说法不正确的是 ( )
 食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益,其分子结构如图所示.下列说法不正确的是 ( )
食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益,其分子结构如图所示.下列说法不正确的是 ( )| A. | 油酸的分子式为C18H34O2 | |
| B. | 油酸可与氢氧化钠溶液发生中和反应 | |
| C. | 1 mol油酸可与2 mol H2发生加成反应 | |
| D. | 1 mol甘油可与3 mol油酸发生酯化反应 |
4.下列说法中错误的是( )
①互为同系物的物质通式相同
②分子组成上相差一个或几个CH2原子团的有机物一定是同系物
③若两种烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同系物的两种有机物的物理性质有差异,但化学性质必定相似.
①互为同系物的物质通式相同
②分子组成上相差一个或几个CH2原子团的有机物一定是同系物
③若两种烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同系物的两种有机物的物理性质有差异,但化学性质必定相似.
| A. | ①②③④ | B. | ②③ | C. | ③④ | D. | ①②③ |
8.下列分子中各原子都满足了8电子稳定构型的是( )
| A. | H2O | B. | SF4 | C. | BF3 | D. | PCl3 |
5.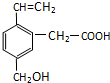 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )
①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能使溴水褪色;
⑥能发加成反应.
 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能使溴水褪色;
⑥能发加成反应.
| A. | ①④ | B. | 只有⑥ | C. | 只有⑤ | D. | 全部 |
8.在容积不变的密闭容器中加入1mol N2和3mol H2反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,下列结论正确的是( )
| A. | 该反应达到平衡时,放出的热量等于92.4kJ | |
| B. | 达到平衡后向容器中通入1mol氦气,容器内压强增大,平衡向右移动 | |
| C. | 降低温度和缩小容器体积均可使该反应的平衡常数增大 | |
| D. | 若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90% |
 .
.
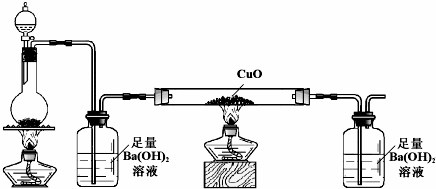
 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下: